Озоноразрушающие вещества и экологически безопасные альтернативы
До тех пор, пока не было обнаружено, что озоновый слой разрушается вследствие выбросов в атмосферу хлорфторуглеродов (ХФУ), эти вещества активно использовались в холодильной и климатической технике.
В 1990-х годах в холодильном и климатическом оборудовании, а также в производстве пеноматериалов стали активно применяться гидрохлорфторуглероды (ГХФУ), рассматривавшиеся в то время в качестве вполне приемлемой переходной альтернативы ХФУ. Эти озоноразрушающие вещества были включены в Приложение С к Монреальскому протоколу, и для них были установлены меры регулирования. Предполагалось, что использование ГХФУ, являющихся, как и ХФУ, озоноразрушающими веществами, но имеющих значительно меньший, чем у ХФУ, озоноразрушающий потенциал (ОРП), будет временной мерой, а в последующем их производство и потребление также будет ликвидировано в рамках Монреальского протокола. Однако опасность ГХФУ заключается не только в их способности разрушать озоновый слой, но и в том, что они обладают высоким потенциалом глобального потепления (ПГП), и на основании этого отнесены к парниковым газам. Парниковыми газами являются и гидрофторуглероды (ГФУ), рассматривавшиеся ранее в качестве озонобезопасной замены ГХФУ, и их использование способно принести заметный вред окружающей среде. В рамках Проекта ЮНИДО/ГЭФ по поэтапному выводу из оборота ГХФУ предполагается исключить данные озоноразрушающие вещества из производства и осуществить переход на альтернативные холодильные и вспенивающие агенты, не обладающие ПГП.
Подробнее об озоноразрушающих веществах:
- Классификация озоноразрушающих веществ
- Озоноразрушающие вещества (ХФУ и галоны) в Российской Федерации: ХФУ 11, ХФУ 12, ХФУ13, ХФУ 113, ХФУ 115, Галон 2402, Галон 1211, Галон 1301
- Переходные озоноразрушающие вещества или гидрохлорфторуглероды: ГХФУ 21, ГХФУ 22, ГХФУ 141b, ГХФУ 142b
- Применение ХФУ и ГХФУ в различных секторах потребления
Экологически безопасные альтернативы:
Аммиак (R717)
Аммиак не является газом, разрушающим озоновый слой (ОРП = 0), он также не вносит прямого вклада в увеличение парникового эффекта (ПГП = 0). По термодинамическим свойствам аммиак – один из лучших хладагентов: по объемной холодопроизводительности он значительно превышает R12, R11, R22 и R502, имеет более высокий коэффициент теплоотдачи, что позволяет применять в теплообменных аппаратах трубы меньшего диаметра.
Пары аммиака легче воздуха, он хорошо растворяется в воде (один объем воды может растворить 700 объемов аммиака, что исключает замерзание влаги в системе).
Из-за резкого запаха аммиака появление течи в холодильной системе легко обнаруживается органолептически обслуживающим персоналом. Кроме того, хладагент R717 имеет низкую стоимость, т.к. объемы его производства (для иных нужд) значительны.
Особенность аммиака как хладагента – более высокое значение температуры нагнетания по сравнению с R22 и R12. В связи с этим предъявляются жесткие требования к термической стабильности холодильных масел, используемых в сочетании с аммиаком в течение длительного времени при эксплуатации установки. Конденсатор должен иметь развитую поверхность теплообмена, в результате чего возрастает его металлоемкость.
Диоксид углерода (R744)
Углекислый газ (СО 2) – дешевое нетоксичное, негорючее и практически экологически чистое вещество (ОРП = 0, ПГП = 1). Его преимущества: низкая цена, простое обслуживание, совместимость с минеральными маслами, электроизоляционными и конструкционными материалами. Вместе с тем, при использовании диоксида углерода требуется водяное охлаждение конденсатора холодильной машины, увеличивается металлоемкость холодильной установки (по сравнению с металлоемкостью установок, работающих на галоидопроизводных хладагентах). Перспективно применение диоксида углерода в низкотемпературных двухкаскадных установках и системах кондиционирования воздуха автомобилей и поездов, а также в бытовых холодильниках и тепловых насосах.
Кроме того, диоксид углерода (в жидком виде и в смеси с водой) может применяться для получения эластичных и эластомерных пен.
Пропан (R290)
Пропан нетоксичен, характеризуется низкой стоимостью, имеет хорошие экологические характеристики (ОРП = 0, ПГП = 3). При использовании данного хладагента не возникает проблем с выбором конструкционных материалов деталей компрессора, конденсатора и испарителя. Пропан хорошо растворяется в минеральных маслах.
Принципиальный недостаток пропана – пожароопасность. Кроме того, габариты компрессора при использовании пропана будут больше, чем у компрессора аналогичной холодопроизводительности на R22.
Пропан можно сразу же запускать в систему, где до этого применялся озоноопасный хладагент. Он работает с теми же минеральными маслами, требует такой же электроизоляции, тех же уплотняющих материалов, труб того же диаметра. Как показали исследования, в этом случае теряется до 10% холодопроизводительности, если в системе ранее был R22, и 15% – если R502. Процедура сервисного обслуживания практически не изменяется.
Изобутан (R600a)
Этот природный газ не является разрушителем озона и озонового слоя (ОРП = 0) и не способствует появлению парникового эффекта (ПГП = 0,001). Масса хладагента, циркулирующего в холодильном агрегате при использовании изобутана, значительно сокращается (примерно на 30%). Изобутан хорошо растворяется в минеральном масле, имеет более высокий, чем R12, холодильный коэффициент, что приводит к снижению энергопотребления.
При этом изобутан горюч, легко воспламенятся и взрывоопасен в соединении с воздухом при объемной доле хладагента 1,3…8,5%. Температура возгорания равна 460oС.
В настоящее время R600a широко применяется в бытовой холодильной технике. В частности, компрессоры, работающие на изобутане, выпускает международный концерн Electrolux. Холодильные агрегаты с R600a характеризуются меньшим уровнем шума из-за низкого давления в рабочем контуре хладагента.
Также изобутан может применяться в качестве вспенивающего агента для получения полиуретановых пен.
Циклопентан
Использование циклопентана в качестве вспенивающего агента при получении жестких полиуретановых изоляционных пенопластов началось в 90-х годах. Переход на циклопентан обусловлен его экологичностью. Однако из-за более высокой температуры кипения и худшего коэффициента теплопроводности он уступает по эффективности R11. Уменьшение прочности при сжатии готовых пенопластов обычно приводит к повышению плотности изделий и трудностям при формовании. Увеличение веса пены, высокая стоимость циклопентана, затраты на переоборудование предприятия, связанные с безопасностью работы с горючими вспененными агентами, приводят к росту издержек производства. Кроме того, такие летучие органические соединения, как циклопентан, могут способствовать образованию фотохимического смога, в котором проходят реакции, приводящие к образованию тропосферного озона – третьего по степени влияния на климат парникового газа.
Презентации и программное обеспечение
Дополнительные материалы
Перейти к странице «Европейский опыт F-регулирования»
www.ozoneprogram.ru
Антарктика: зафиксирован рост запрещенных озоноразрушающих веществ.
Концентрация озона в атмосфере чрезвычайно мала — 3 молекулы озона на 10 млн. молекул воздуха. Но несмотря на такой незначительный объем, озоновый слой играет жизненно важную роль. Дело в способности молекул озона поглощать ультрафиолетовое излучение. Опасные для живых организмов лучи UVC, повреждающие ДНК-клеток, и часть спектра лучей UVB полностью поглощаются озоновым слоем и не достигают поверхности Земли.
Озоновый слой
Около 90% озона сосредоточено в слое на высоте от 20 до 30 км над поверхностью Земли. Толщина озонового слоя и высота над поверхностью Земли меняется сезонно и зависит от широты. В полярных широтах озоновый слой «толще» и находится на высоте, начиная от 15 км над поверхностью.
Озон (О3) представляет трёхатомную молекулу кислорода. Под воздействием ультрафиолетового излучения молекулярный кислород (О2) распадается на атомы (О). Атомарный кислород в свою очередь, соединяясь с молекулярным кислородом, образует озон. Затем вновь поглощая ультрафиолетовое излучение озон распадается на молекулярный и атомарный кислород с выделением тепла. Образуется озоно-кислородный цикл, при котором происходит конверсия наиболее опасной части спектра ультрафиолетового излучения в тепло. Роль озона незаменима: молекулы озона отличаются наибольшей интенсивностью поглощения в отличие от составляющих его атомов (когда они существуют по отдельности), так и двухатомных молекул О

Озоноразрушающие вещества
К распаду озона могут также вести реакции и с другими элементами атмосферы: с оксидом азота, хлором и бромом. Большинство этих веществ естественно присутствуют в атмосфере и озоно-кислородный цикл сбалансирован. Но активность человека может приводить к нарушению баланса. Выбросы хлорфторуглеродов значительно увеличили концентрацию хлора в атмосфере. Озоноразрушающие вещества входят в состав холодильных агентов, пенообразователей, средств пожаротушения, растворителей, средств обработки сельхозпродукции, участвуют в процессах производства труб и плит теплоизоляции. Каждый атом хлора может разрушать до нескольких десятков тысяч молекул озона.

Почему озоновые дыры образуются в полярных широтах?
Озон образуется, в основном, в зонах с высокой инсоляцией — в экваториальной зоне в верхней стратосфере. Затем благодаря циркуляции воздуха в верхних слоях атмосферы переносится к полюсам, где он может накапливаться. Кроме того, вместе с глобальной циркуляцией воздуха переносятся и вредные примеси — хлорсодержащие вещества.
Из-за аномально низких температур в течение зимы в полярных стратосферных облаках происходят химические реакции, в результате которых накапливаются нестабильные соединения, содержащие хлор и бром, катализирующие разрушение озона. При первых солнечных лучах происходит запуск реакций разрушения озона. Процесс происходит до тех пор, пока температура не вырастет настолько, что облака разрушатся, и условия для активного разрушения озона исчезнут.
По этой причине «озоновая дыра» — область в озоновом слое с наименьшей концентрацией, фиксируется каждый год в течение «антарктической» весны с сентября до начала декабря над Антарктикой. На мысе Горн солнцезащитный крем тоже нужен.

Монреальский протокол
Ведущие государства мира в 1988 г. подписали Монреальский протокол, ограничивающий выбросы хлорсодержащих соединений. Использование наиболее опасных фреонов было сокращено. Протокол имел успех, и в 2013 году наметилась тенденция к небольшому уменьшению озоновых дыр с полным восстановлением уровня озона к 2070 году.
Но недавние замеры зафиксировали всплеск озоноразрушающих веществ в атмосфере, несмотря на международные запреты. Циркуляцию воздуха из тропосферы в стратосферу сложно отследить, но исследователи полагают, что источник выбросов находится в восточной Азии.

www.mytransat.com
8.3.2. Соединения, разрушающие озоновый слой
Фреоны. В 1930 г. инженер Т. Мидгли предложил использовать хлорфторуглеводороды в качестве нетоксических компонентов при производстве домашних холодильников. Торговое название их — фреоны (ОиРоп.1). Они отличались рядом уникальных свойств: были негорючими компонентами, не вызывали коррозии металлов. Но самое главное, они кипели при комнатной температуре и легко переходили из жидкого состояния в газообразное и обратно (табл. 8.2). В силу этих свойств фреоны быстро заменили ядовитый аммиак и диоксид серы, которые применялись в качестве охлаждающих жидкостей (хладоагентов).
Таблица 8.2
Химические свойства некоторых хлорфторуглеводородов
Название | Формула | Давление пара, атм | Температура, кипения, °С | |
-13 °С | 27 °С | |||
Фреон-11 | СРС1, | 0,22 | 1,12 | 23,8 |
Фреон-12 | СР2С12 | 1,93 | 6,75 | -29,8 |
Фреон-113 | СРС12СС1Р2 | 0,08 | 0,47 | 47,4 |
Помимо холодильной техники, фреоны широко применяются при производстве аэрозолей (пропелленты), вспенивающих веществ при производстве пенополиуретанов, в электронной промышленности для очистки деталей электронного оборудования. Сюда относятся трифторметан — К11, дихлордифторметан — К12, хлордифторметан — К22, дихлорфторэтан — К1415, пентафторэтан — К125, тетрафтор-этан — К.134а.
Фреон-12 долгое время был основным хладоагентом в домашних холодильниках, а фреон-22 — в домашних кондиционерах. Фреон-11 используется в производстве пластмасс. Наибольшей способностью воздействовать на озон стратосферы обладают фреон-11 и фреон-12, наименьшей — фре-он-125 и фреон-134а. Особенно существен вклад в загрязнение воздушной среды фреонов, используемых в качестве пропеллентов для аэрозольных упаковок. В табл. 8.3 представлены данные об озоноразрушающей активности основных фреонов.
Таблица 8.3
Озоноразрушающий потенциал некоторых соединений
Соединение | Разрушающий потенциал, усл. ед. | Продолжительность жизни, годы |
Фреон-11 | 1,00 | 75 |
Фреон-12 | 1,00 | 111 |
Фреон-113 | 0,80 | 90 |
Фреон-114 | 1,00 | 185 |
Фреон-115 | 0,60 | 380 |
Четыреххлористый углерод | 1,06 | 50 |
Галон-1301 | 10,00 | 110 |
НСРС-22 | 0,05 | 20 |
В настоящее время мировое производство фреонов превышает 1 млн т в год (рис. 8.3). Подсчитано, что около 85% фреона-11 и фреона-12, произведенных к настоящему времени, уже попало в атмосферу. В последние 15 лет ежегодный общемировой выброс в атмосферу фреона-12 находился в диапазоне 350—500 тыс. т, фреона-11 — 250— 400 тыс. т.
Россия + страны Восточной Европы
Фреоны — долгоживущие молекулы (в атмосфере могут находиться до нескольких сотен лет), не растворимы в воде,летучи. В области экватора из-за наличия мощных восходящих потоков воздуха фреоны могут попадать в стратосферу. Там под действием УФИ от фреонов отделяется атомарный хлор, который, взаимодействуя с озоном, образует молекулярный кислород и активный СЮ. Взаимодействие последнего с атомарным кислородом приводит к образованию кислорода и вновь атома хлора, который продолжает процесс разрушения озона (рис. 8.4).
Четыреххлористый углерод (СС14). Широко применяется в химической промышленности.
Расчеты показывают, что один атом хлора способен разрушить до 10 тыс. молекул озона. Это приводит к образованию так называемых озоновых дыр (рис. 8.5).
Соединения брома. Некоторые из этих компонентов производятся в промышленных масштабах. Сюда относятся так называемые талоны (например, СР3Вг) — действующее вещество химических огнетушителей, а также метилбромид, используемый в сельском хозяйстве как фумигант. При этом следует учитывать, что атомы брома являются в 50 раз более активными в разрушении озона, чем другие соединения.
Соединения азота (>ЮХ). Эти компоненты образуются при распаде химически стабильного 1Ч20 при посредстве почвенных микроорганизмов. N0 и >Ю2 имеют дополнительные электроны, следовательно, являются свободными радикалами и весьма активны. Хотя их концентрация невелика, за время своего существования они способны разрушить тысячи молекул озона.
Помимо этого, источниками оксидов азота в стратосфере являются реактивные самолеты, пуски ракет, а также использование азотных удобрений в сельском хозяйстве и сжигание ископаемого топлива.
Соединения водорода. К этой группе соединений можно отнести гидроксиды ОН». Их источниками являются реактивные самолеты, выбрасывающие при сжигании топлива пары воды, а также пары воды, попавшие из тропосферы.
Соединения серы. Одним из мощных источников серы в стратосфере является вулканическая деятельность.
studfiles.net
6. Назовите источники поступления в атмосферу веществ, разрушающих озоновый слой
Запуск мощных ракет, ежедневные полеты реактивных самолетов в высоких слоях атмосферы, испытания ядерного и термоядерного оружия, ежегодное уничтожение природного озонатора — миллионов гектаров леса — пожарами и хищнической рубкой, массовое применение фреонов в технике, парфюмерной и химической продукции в быту — главные факторы, разрушающие озоновый экран Земли.
В последние годы над Северным и Южным полюсами возникли «озоновые дыры» площадью свыше 10 млн. км2 каждая, появились громадные «озоновые дыры» над многими странами Европы, над Россией. Разрушение озонового экрана Земли сопровождается рядом опасных явных и скрытых негативных воздействий на человека и живую природу.
Прорыв через «озоновые дыры» солнечных рентгене- и ультрафиолетовых лучей, энергия фотонов которых превышает энергию лучей видимого спектра в 50—100 раз, увеличивает число мощных лесных пожаров. В 1996 г. в России сгорело 1 млн. га леса, горели леса в Австралии, Северной и Южной Америке, Африке, Европе, в Юго-Восточной Азии. Индонезийский лесной пожар 1997 г., бушевавший почти пять месяцев, покрыл дымом не только Индонезию, но и Малую Азию, Сингапур, достиг Южно-Китайского моря. Люди задыхались от дыма, потерпел катастрофу авиалайнер.
В 1996 г. Нобелевской премией по химической экологии удостоены ученые-химики Шервуд Роуланд, Марио Малина из Калифорнийского университета в Беркли (США) и Поль Крутцен из Германии за научную гипотезу, выдвинутую ими еще в 1974 г. Их догадка состоит в том, что разрушителями озона являлись синтезированные человеком химические вещества, получившие название хлорфторуглероды (ХФУ).
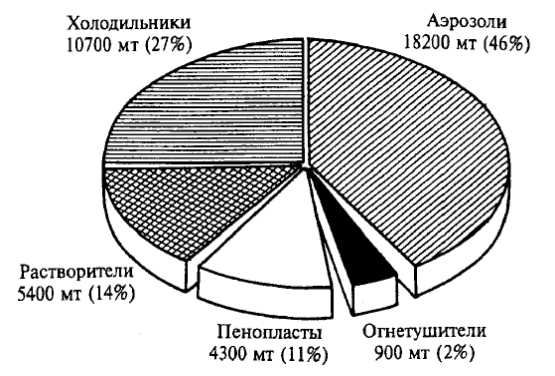
На рисунке представлена диаграмма потребления озоноразрушающих веществ (ОРВ) в России в 1992 г. Инертные, негорючие, неядовитые, несложные в производстве, они получили широкое распространение — в баллончиках с аэрозолями различного назначения, а также как охлаждающие жидкости в холодильниках и кондиционерах, как растворители (тетрахлорметан, метилхлороформ, бромистый метил), в производстве пестицидов. Бромистый метил используется в качестве дезинфицирующего вещества для почв и товаров (включая карантинную обработку некоторых продуктов, предназначенных для международной торговли), применяется в качестве добавки к автомобильному топливу. Из бромистого метила высвобождается бром, который в 30-60 раз разрушительнее для озона, чем хлор. Другие химические соединения, разрушающие озоновый слой, используются в баллонах для тушения пожара, при изготовлении полистироловых стаканчиков и современных упаковок для фасовки продуктов и полуфабрикатов.
Пик мирового производства ОРВ пришелся на 1987—1988 гг. и составил около 1,2—1,4 млн. т в год. Около 35% производимого объема приходилось на США, 40% — на страны ЕЭС, 10—12% производила Япония, 7-10% — наша страна.
Механизм действия фреонов таков: попадая в верхние слои атмосферы, эти вещества, инертные у земной поверхности, преображаются. Под воздействием ультрафиолетового излучения химические связи в молекулах ХФУ нарушаются. В результате выделяется хлор, который при столкновении с молекулой озона вышибает из нее один атом. Озон перестает быть озоном, превращается в обычный кислород. Хлор же, соединившись временно с кислородом, вскоре опять оказывается свободным и «пускается в погоню» за следующей «жертвой». Его активности хватает, чтобы разрушить десятки тысяч молекул озона.
studfiles.net
Ученые выявили вещества, разрушающие озоновый слой «не хуже» фреона
Британские ученые обнаружили в атмосфере Земли ранее неизвестный класс химических веществ
«Нам нужно продолжить наблюдения за состоянием атмосферы и концентрацией этих газов для того, чтобы определить их источник. Сейчас озоновый слой все еще испытывает благоприятные эффекты от запрета фреонов, но растущая концентрация дихлорметана в атмосфере может нейтрализовать их и внести массу неопределенностей в наши прогнозы по будущему состоянию озона и климата», — заявил Мартин Чипперфилд из университета Лидса.
Он и его коллеги раскрыли новый класс органических веществ, разрушающих озоновый слой, наблюдая за изменениями в концентрации антропогенных и природных соединений, содержащих в себе атомы галогенов — хлора, брома, йода.
Как отмечают исследователи, подобные молекулы широко встречаются в природе и промышленности и они легко разрушают озон, однако экологи не обращали на них особого внимания из-за того, что они распадаются очень быстро и живут в атмосфере не дольше полугода. По этой причине ученые часто называют их VSLS — «короткоживущими субстанциями».
Исследователи решили проверить, насколько высока их концентрация в воздухе сегодня и влияют ли они, хоть в какой-либо степени, на состояние озонового щита в стратосфере Земли. Первые же замеры показали, что доля VSLS в воздухе была не просто высокой, но и достаточно быстро росла на протяжении последних 20 лет. В некоторых уголках планеты, отмечают ученые, их концентрация выросла в два раза, а в целом доля содержащих хлор веществ из этого класса в 50 раз больше, чем концентрация хлоровых фреонов в атмосфере.
По расчетам ученых, на долю человека пока приходится лишь 10% от общего числа молекул озона, уничтоженных VSLS, но их «вклад» в разрушение озонового слоя продолжает расти. Кроме того, эти вещества разлагают озон не только в стратосфере, где находится озоновый слой, но и в нижней части атмосферы, что может заметным образом влиять на климат планеты (озон является сильным парниковым газом).
Эксперты выделили естественные источники очень короткоживущих субстанций, например, морские водоросли, и промышленные источники, чтобы выяснить вклад каждой из групп, отмечает innovanews.ru. Итак, сегодня естественно выделяемые VSLS по сравнению с промышленными разрушают озон в соотношении 9 к 1. Но вклад промышленных источников растет и продолжит увеличиваться с годами.
Считается, что причиной уменьшения озона в стратосфере и образование озоновых дыр является производство и применение хлор- и бромсодержащих фреонов. Попадая после использования в атмосферу, они разлагаются под воздействием ультрафиолетового излучения Солнца. Высвободившиеся компоненты активно взаимодействуют с озоном в так называемом галогеновом цикле распада атмосферного озона.
Подписание и ратификация странами ООН Монреальского протокола привело к уменьшению производства озоноразрушающих фреонов и способствует восстановлению озонового слоя Земли.
В связи с пагубным влиянием озоноразрушающего фреона R-22, его использования год от года сокращается в США и Европе, где с 2010 года официально запрещено применять этот фреон. В России c 2011 года прекращен импорт холодильного оборудования, в том числе кондиционеров промышленного и полу-промышленного класса, однако сам фреон пока производится в стране. На замену фреону R-22 должен прийти фреон R-410A, а также ретрофиты R-407C, R-422D.
www.mk.ru
Какие пять вещей, разрушают озоновый слой? -Great.Az
Озоновый слой, который находится в стратосфере, в 20 — 50 километрах над поверхностью Земли, имеет решающее значение для существования человека, потому что он защищает людей от вредного воздействия ультрафиолетовых лучей исходящих от солнца. В 1970-х годах, исследования доказали, что химические вещества, производимые в сфере коммерческой деятельности приводит к разрушения озонового слоя. К озона-разрушающим веществам (ОРВ) относятся Хлорфторуглероды, Бромистый метил, Галона соединения(Галоны — это малотоксичные и химически устойчивые соединения) и метилхлороформ.Хлорфторуглероды
Хлорфторуглеродовое (ХФУ) соединение, состоит из хлора, фтора и углерода. Они являются побочным продуктом химических веществ, используемых в производственной деятельности, таких как промышленные растворители, электронные очистители и хладагенты. Когда она достигает стратосферы, соединение распадается на более простые вещества, в результате разрушается озоновый слой.
Гидрохлорфторуглероды
Гидрохлорфторуглеродовое (ГХФУ) соединение содержащее водород, хлор, фтор и углерод, используется в промышленности как альтернатива ХФУ. Как ХФУ, ГХФУ также содержат хлор, который, достигнув стратосферы, освобождаются атомы хлора, разрушающие озоновый слой. Однако воздействие ГХФУ на озоновый слой, все же меньше, чем ХФУ.
Бромистый метил
Бромистый метил может быть «синтетическим» состоящим из химических соединений или «природным соединением» выпускаемый водорослями в океане. Первоначально использовался как мощный пестицид.
Ультрафиолетовое излучение разбивает его, когда он достигает стратосферы, что приводит к разрушению озонового слоя. Помимо того, что это опасно для окружающей среды, он также может быть вредным для здоровья человека.
Галон
Соединение галонов содержит фтор и углерод, а также бром. Он широко используется в качестве огнетушащего вещества. Бром вызывает больше повреждения озонового слоя, чем хлор.
Метилхлороформ
Метилхлороформ является синтетическим соединением химических веществ, используемый в нескольких промышленных отраслях в качестве клея и растворителя, а также используется в переработке отходов. Он также находится в нескольких потребительских товарах, таких как краски и чистящие средства. Метилхлороформ также непосредственно опасен для здоровья человека, влияя на глаза, печень, сердце, легкие и кожу.
great.az
Монреальский протокол по веществам, разрушающим озоновый слой
16 сентября 1987 года в Монреале (Канада) представители 46 стран подписали Монреальский протокол по веществам, разрушающим озоновый слой.
К этому времени уже была выяснена роль атомов хлора и брома в истощении слоя озона в стратосфере, и в приложения к протоколу были включены хлорфторуглероды (ХФУ) и бромсодержащие галоны.
В Статье 5 Монреальского протокола оговаривается особое положение развивающихся стран. К ним относятся страны с расчетным уровнем ежегодного потребления озоноразрушающих веществ (ОРВ) менее 0,3 кг на душу населения. Остальные страны с точки зрения протокола считаются развитыми.
Изначально Монреальский протокол 1987 года предусматривал замораживание производства пяти наиболее применяемых ХФУ и галонов на уровне 1986 года, а затем сокращение их производства на 20 % к 1993 году и на 30 % — к 1998 году. Документ ограничивал экспорт и импорт ОРВ, а также предполагал помощь развивающимся странам по переводу промышленности на озонобезопасные вещества и технологии.
Итогом реализации мер, предусмотренных Монреальским протоколом, должно было стать значительное снижение объемов мирового производства ОРВ, но не его полное прекращение. Тем самым промышленности предоставлялось время на разработку и внедрение технически и экономически приемлемых альтернатив (ТЭПА).
Позднее поправки и корректировки к протоколу расширили перечень контролируемых веществ, сроки прекращения их производства и потребления, а также меры по ограничению экспортно-импортных и других операций.
По состоянию на сентябрь 2018 года сторонами Монреальского протокола являются 197 стран.
Советский Союз подписал протокол 29 декабря 1987 года и ратифицировал 10 ноября 1988 года. Российская Федерация является Стороной Монреальского протокола с 31 декабря 1991 года.
Некоторые положения Монреальского протокола
Статья 2 устанавливает график поэтапного прекращения производства и потребления ОРВ.
Статья 3 определяет порядок расчета регулируемых уровней.
Статья 4 описывает меры по контролю торговли ОРВ, которые должны стимулировать страны присоединяться к Монреальскому протоколу и предотвращать передачу ОРВ, произведенных в обход мер регулирования, странам, не являющимся Сторонами Монреальского протокола.
Статья 5 предоставляет развивающимся странам с уровнем потребления ОРВ ниже установленного предела право отложить соблюдение мер регулирования, предусмотренных в статье 2, на 10 лет.
Статья 6 предписывает не реже одного раза в 4 года пересматривать меры регулирования на основе самой свежей информации о научных, экологических, технических и экономических аспектах разрушения озонового слоя.
Статья 7 предусматривает ежегодное представление статистических данных о производстве, импорте и экспорте каждого из регулируемых веществ в Озоновый секретариат.
Статья 8 устанавливает введение мер по определению факта несоблюдения положений Монреальского протокола.
Статья 9 предусматривает обмен информацией между Сторонами.
Статья 10 предусматривает предоставление технической помощи развивающимся странам на справедливых и наиболее благоприятных условиях.
Применяемый для этого механизм финансирования включает формы многостороннего, регионального и двустороннего сотрудничества, а также Многосторонний фонд для осуществления Монреальского протокола. Из средств МФМП покрываются «согласованные дополнительные расходы», которые развивающиеся страны, действующие в рамках пункта 1 статьи 5, несут в связи с соблюдением мер регулирования, предусмотренных Монреальским протоколом.
Поправки и корректировки к Монреальскому протоколу
Первая редакция протокола была одобрена 16 сентября 1987 года и вступила в силу 1 января 1989 года.
В протоколе предусмотрено положение о корректировках расчетных коэффициентов с учетом последних научных данных, которое позволяет оперативно изменять график вывода регулируемых веществ. Корректировки автоматически распространяются на все страны, ратифицировавшие протокол.
Протокол также предусматривает поправки, которые подлежат ратифицикации Сторонами. За время действия протокола были приняты Лондонская, Копенгагенская, Монреальская, Пекинская и Кигалийская поправки.
Помимо корректировок и поправок ежегодно проходят заседания Сторон протокола, на которых принимаются решения по его реализации.
Лондонская поправка
В соответствии с Лондонской поправкой в список ОРВ включили ряд новых ХФУ, а также метилхлороформ (МХФ) и четыреххлористый углерод (ЧХУ).
Также был введен термин «переходные вещества», т. е. соединения, оказывающие воздействие на озоновый слой, срок производства которых не был ограничен. Эти вещества рассматривались в качестве ТЭПА и включали гидрохлорфторуглероды (ГХФУ) и их бромсодержащие аналоги гидробромхлорфторуглероды (ГБФУ).
Лондонская поправка была принята решением II Совещания Сторон Монреальского протокола (г. Лондон, 27–29 июня 1990 года). По состоянию на сентябрь 2018 года Лондонская поправка ратифицирована всеми 197 Сторонами Монреальского протокола.
СССР принял ее во исполнение постановления Кабинета Министров СССР от 23.04.1991 № 198. Она вступила в силу для Российской Федерации после сдачи ратификационной грамоты 13 января 1992 года.
Копенгагенская поправка
Поправка установила срок прекращения производства ГХФУ (2030 и 2040 год для стран статьи 2 и 5 соответственно) и ГБФУ (1996 год) и перенесла сроки прекращения производства пяти ХФУ (хладагентов R11, R12, R113, R114, R115), ЧХУ, МХФ (1996 год) и галонов (1994 год).
В число ОРВ, регулируемых протоколом, был введен метилбромид (бромистый метил). Потребление этого фумиганта было заморожено на уровне 1995 года для Сторон статьи 2 и 2002 года для Сторон статьи 5.
Копенгагенская поправка была принята на IV Совещании Сторон Монреальского протокола (г. Копенгаген, 23–25 ноября 1992 года) и по состоянию на сентябрь 2018 года ратифицирована всеми 197 Сторонами Монреальского протокола.
Российская Федерация является Стороной Копенгагенской поправки к Монреальскому протоколу с 14 декабря 2005 года.
Монреальская поправка
Поправка предусматривает создание глобальной системы лицензирования и регулирования импорта и экспорта ОРВ, корректирует график прекращения производства метилбромида, а также вводит запрет на импорт и экспорт этого вещества в страны и из стран, не являющихся Сторонами Копенгагенской поправки с 10 ноября 2000 года.
Поправка была принята на IX Совещании Сторон Монреальского протокола (г. Монреаль, 15–17 сентября 1997 года) и по состоянию на сентябрь 2018 года ратифицирована всеми 197 Сторонами Монреальского протокола.
Российская Федерация является Стороной Монреальской поправки к Монреальскому протоколу с 14 декабря 2005 года.
Пекинская поправка
Пекинская поправка устанавливает новые уровни потребления ГХФУ, запрещает торговлю любыми ОРВ со странами, не ратифицировавшими данную поправку, вводит меры регулирования производства ГХФУ, ХФУ и галонов для развивающихся стран, а также запрещает производство и потребление бромхлорметана с 1 января 2002 года. Производство ГХФУ, в частности, было заморожено на уровне 1 января 2004 года для Сторон статьи 2 и на уровне 1 января 2016 года для Сторон статьи 5.
Поправка была принята решением XI Совещания Сторон Монреальского протокола (г. Пекин, 29 ноября — 3 декабря 1999 года) и по состоянию на сентябрь 2018 года ратифицирована всеми 197 Сторонами Монреальского протокола.
Российская Федерация является Стороной Пекинской поправки к Монреальскому протоколу с 14 декабря 2005 года.
Кигалийская поправка
Эта поправка предусматривает поэтапное сокращение производства и потребления гидрофторуглеродов (ГФУ).
Она добавляет 100-летний ПГП для ряда ГХФУ и вводит в текст протокола Приложение F, включающее ГФУ. Расчеты объемов потребления (в том числе базовый уровень) в рамках поправки производятся не в тоннах озоноразрушающей способности, а в тоннах ПГП.
Поправка также устанавливает отдельные графики сокращения потребления ГФУ для четырех групп государств: двух групп развивающихся стран и двух развитых.
Кигалийская поправка была принята на XXVIII Совещании Сторон Монреальского протокола (г. Кигали, 10–15 октября 2016 года) и по данным на конец сентября 2018 года ратифицирована 48 Сторонами Монреальского протокола.
Она вступает в силу 1 января 2019 года за исключением положения, касающегося мер по регулированию в сфере торговли ГХФУ, которое вступает в силу 1 января 2033 года, если поправку ратифицируют не менее 70 Сторон протокола.
Текущие обязательства РФ по Монреальскому протоколу
| Вещество | Период | Сокращение относительно базового уровня, % | Ежегодное потребление регулируемых веществ, тонна ОРС |
|---|---|---|---|
| ГХФУ | 01.01.2015‑31.12.2019 | 90,0 | 399,69 |
| 01.01.2020‑31.12.2029 | 99,5 | 19,98 | |
| С 01.01.2030 | 0 | 0 |
Тонна ОРС — тонна озоноразрушающей способности.
Базовый уровень ГХФУ — 3999,9 тонны ОРС.
Ожидаемые обязательства РФ по Монреальскому протоколу
В случае ратификации Кигалийской поправки Россия будет обязана выводить ГФУ из обращения по следующему графику:
| Вещество | Период | Сокращение относительно базового уровня, % | Ежегодное потребление регулируемых веществ, тонны ПГП |
|---|---|---|---|
| ГХФУ | 01.01.2020‑31.12.2024 | 95 | Не определено |
| 01.01.2025‑31.12.2028 | 65 | Не определено | |
| 01.01.2029‑31.12.2033 | 30 | Не определено | |
| 01.01.2034‑31.12.2035 | 20 | Не определено | |
| С 2036 года | 15 | Не определено |
Тонна ПГП — тонна потенциала глобального потепления.
Базовый уровень ГФУ — равен среднему потреблению ГФУ в 2011–2013 годах плюс 25 % от базового уровня ГХФУ.
Многосторонний фонд для осуществления Монреальского протокола был организован в 1991 году для помощи развивающимся странам в выполнении обязательств по Монреальскому протоколу. Подробнее
Озоновый секретариат — это секретариат Венской конвенции об охране озонового слоя и Монреальского протокола по веществам, разрушающим озоновый слой. Подробнее
www.ozoneprogram.ru
