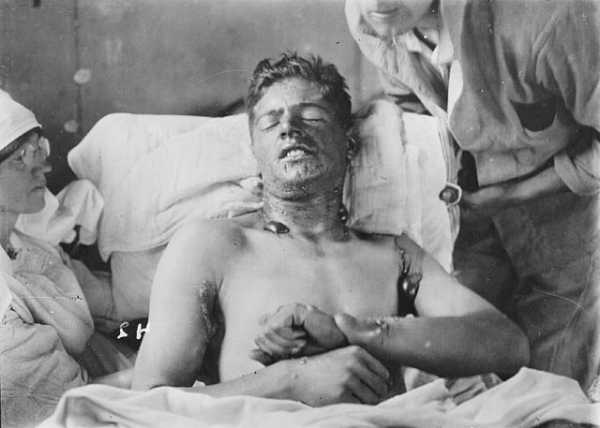
Как иприт начал лечить рак (более-менее) / Habr
Недавно случайно разговорился в поликлинике с человеком, больным лейкозом, и меня это подтолкнуло к мысли написать немного об одних из первых, и до сих пор главных, химиотерапевтических препаратах лечения рака. А самое главное – как они были созданы.Но сначала немного об ипритах. Иприт далеко не один, их несколько и о них о всех я расскажу.
Первый иприт, примененный сначала немцами, а потом Союзниками в Первую мировую — 2,2′-дихлордиэтилсульфид — имел формулу – S(C2h5Cl)2 или
Само применение ОВ не означает, что им просто «заливают» противника при помощи артобстрела, на самом-же деле, каждое ОВ имеет свою тактическую нишу, зачастую очень узкую. Тактическая ниша иприта – делать какую-то местность недоступной или хотя-бы малодоступной на относительно долгий период. Иприт крайне ядовит, даже небольшая его капля оставшаяся на одежде выведет из строя не только владельца одежды, но и любого, кто будет находиться с ним в одном помещении. При этом его дегазация весьма трудоемка – иприт растворяется и всасывается почти во все материалы – от кирпича до резины. В частности, этим обусловлена двухчасовая норма нахождения в одном противогазе на местности, зараженной ипритом. Однако, даже в идеальных условия продегазировать иприт не столь уж и просто – он довольно медленно взаимодействует с растворами хлорной извести, его дегазация требует перемешивания т.к. он является маслоподобным веществом. В качестве примера, привожу воспоминания некой Н.М.Годжелло из книги Л. Федорова (главный человек в России по проблемам химического оружия):
«Мой папа, артиллерист по образованию, служил после революции начальником артсклада в Одессе, а в 1923 году был откомандирован в Москву, где получил назначение на службу на химический полигон в Кузьминки. Вскоре папа получил ипритное поражение: при вскрытии снаряда капля попала на сапог, он не заметил, да и не знал, наверное, что это такое. Три месяца он просидел на веранде (было лето) с вытянутой ногой, на подъеме которой была страшная язва. Я слышала обрывки разговоров с сослуживцами, которые навещали его и обсуждали коварные свойства иприта. Позднее папа рассказал мне, что в задачу его и его коллег входило разобраться с трофейными снарядами — их конструкцией и чем они начинены. Параллельно со службой на химполигоне папа учился на химическом факультете МВТУ (в те годы там был химфак).»
Конечно иприт применялся не в чистом виде, да и странно было бы ожидать надписи на снаряде «Иприт». По германской номенклатуре времен 1-й мировой иприт был главной составляющей химических снарядов «желтый крест» заправленных смесью из
При этом к смесям добавлялись какие-либо резко пахнущие отходы предприятий органического синтеза – с одной стороны, «незнакомое» ОВ существенно понижало боевой дух солдат противника, с другой – затрудняло анализ смеси.
Из-за свойств иприта эффективность его применения была очень высока – снарядами с ним обстреливали конечно-же не те позиции противника, которые предстояло занять своим войскам, а те, с которых противника нужно было прогнать. Либо заразить ипритом участок местности, чтобы противник не мог его пересечь. В тактическом смысле это исключительная возможность. Вспомним советские поливальные машины межвоенной эпохи которые конструировались на основе немецкого оборудования для заражения местности ОВ. Оборудование, как и определенная часть технологий по производству ОВ, были переданы СССР Веймарской республикой в конце 1920-х.

Иприт очень, очень ядовит. Хотя данные по его ЛД разнятся и могут показаться относительно невысокими, для ОВ главным является практический результат применения который зачастую кардинально расходится с показателем ЛД. Например, самым сильным ядом считается токсин ботулизма с ЛД50 по современным данным 1.3-2.1*10-9 г/кг. У VX ЛД50 лишь 70*10-6 г/кг т.е. разница, казалось бы, больше четырех порядков. На опытах-же, оказалось, что при заражении местности токсин ботулизма по эффективности уступает VX. Поэтому можно сделать выводы, что иприт пользовался званием «короля ядов» в 1920-х не без оснований. Для иприта главным свойством является яркое цитотоксическое действие – способность вызывать гибель клеток организма с которыми он соприкасается. Попадание иприта на кожу вызывает тяжелый некроз, в районе суставов – поражения, заканчивающиеся потерей суставом подвижности, в глаза – слепоту, прием иприта перорально – вообще говоря, смерть и т.д. Современный взгляд на механизм действия иприта сводится к тому, что он алкилирует ДНК, повреждая ее, в результате чего в клетке включается механизм самоуничтожения. Очень схематично реакция выглядит примерно так:
Как видно, молекула иприта изомеризуется в катион который является кислотой Льюиса, следовательно, нечего необычного в ее реакции с основанием Льюиса — аминогруппой в ДНК — нет.
В Википедии сказано, что иприт алкилирующий агент, что с химической точки зрения не вполне верно. Дело в том, что при обычных химических реакциях своего алкилирующего действия он почти не проявляет – c аммиаком реагирует только при нагревании в запаянной ампуле, с аминами – в присутствии слабого основания, с аминокислотами (являющимися основой белков) взаимодействует очень плохо. Более-менее активно идут реакции лишь с вторичными аминами. Так что можно сказать, что тут с ипритом «повезло» — он достаточно активен для повреждения ДНК, но не слишком активен, чтобы потерять возможность попасть в саму клетку, подвергнувшись гидролизу, плюс его удобные физические свойства (высококипящая жидкость). Из-за этого усилия химиков во многих странах в межвоенный период были посвящены вопросам синтеза иприта, поисков его более ядовитых аналогов и улучшению эксплуатационных свойств. Именно в смысле ядовитости ученых ждал неприятный сюрприз – были найдены многие вещества со схожими с ипритом цитотоксическими свойствами, но сам иприт оказался почти исключительным ядом. Реально принятыми на вооружения оказались лишь т.н. кислородный иприт и азотистый иприт.
Кислородный иприт с формулой
получали сразу в смеси с обычным ипритом действием концентрированной соляной кислоты на тиодигликоль при повышенной температуре (Великобритания). Нечем заметным в истории он не отличился.
Чего нельзя сказать про азотистый иприт, разработки которого активнее всего велись в США (хотя и в Германии под конец войны было обнаружено ок. 2 тыс. тонн азотистого иприта что по меркам ОВ – не очень много). Вспомним формулу иприта в начале. И вот совершенно похожий на него трис(2-хлорэтил)амин хотя и подробно исследованный лишь в середине 1930-х
Действие этого вещества оказалось очень похожим на действие иприта, более того, оно обладало даже определенными преимуществами перед ним. В частности, было гораздо более устойчивым к окислению, следовательно, дегазировать его было труднее чем иприт. Промышленный синтез осуществлялся путем хлорирования триэтаноламина
N(C2h5OH)3 + 3SOCl2 = N(C2h5Cl)3 + 3SO2 + 3HCl
Если кто-то заметил, то триэтаноламин входит в состав многих флюсов для пайки, например ЛТИ-120. На сколько мне известно, хотя триэтаноламин и входит в список прекурсоров для производства ОВ, купить его может каждый желающий. Как и тиодигликоль, кстати, главное сырье для получения обычного иприта. Говоря об триэтаноламине можно заметить, что по ядовитости он конечно очень-очень далек от азотистого иприта, однако, называть его абсолютно безвредным тоже нельзя и он требует осторожности в обращении.
Возвращаясь к азотистому иприту — исследования тогда показали, что наиболее существенным является наличие двух групп -Ch3Ch3Cl у одного атома азота, третья группа может быть и иной. Поэтому были приняты на вооружение еще два азотистых иприта бис(2-хлорэтил)этиламин
и бис(2-хлорэтил)метиламин
Параллельно работам по исследованию хлорэтаноламинов в качестве ОВ, в Йельском университете (США) велись исследования по их-же медицинскому применению. В те времена радиотерапия тоже только-только зарождалась, понятно, что нетрудно провести параллель между действием ионизирующего излучения на организм и действием иприта т.к. в обоих случаях симптомы чем-то схожи. Это, вероятно, натолкнуло А. Гилмана и Л. Гудмана на мысль попробовать лечить рак при помощи иприта. Первыми препаратами которые они в начале 1940-х применили были именно три азотистых иприта, вероятно первым препаратом был бис(2-хлорэтил)метиламин под названиями хлорметин, мехлоретамин, позже в СССР эмбихин. Хотя это вещество до сих пор еще находит применение в медицине не стоит ожидать что тогда произошло чудо – первоначально опухоли уходили, но затем возвращались вновь, причем с потерей чувствительности к хлорметину.
Впрочем, этот препарат все равно позже нашел свою нишу в области лечения лейкоза. Даже не вполне положительный результат был прорывом на тот момент, несколько запоздавшая публикация вызывала волну исследований в области химиотерапевтических противоопухолевых препаратов, особенно производных азотистого иприта. В итоге было синтезировано громадное количество препаратов с все той-же группировкой –N(C2h5Cl)2 или =N(C2h5Cl) которые обладали более существенным действием на опухоль и немного менее разрушительным действием на организм. Тем не менее, опасные свойства азотистого иприта препараты сохраняли.
Занятно, что все иприты являются канцерогенами – за счет повреждения ДНК здоровых клеток они действительно способны провоцировать рак. Иприты входят в 1-ю группу канцерогенов от МАИР т.е. группу веществ, чье канцерогенное действие на человека доказано. В том-же списке находится и тамоксифен – широко применяемое средство против рака молочной железы. Как-же так получается, что препараты которыми лечат рак сами по себе его и вызывают? Это лишь кажущийся парадокс, все абсолютно логично – если вещество вызывает смерть обычных клеток, то оно наверняка будет вызывать и смерть раковых клеток, тем более они более «нежные».
Однажды мне случайно попалось англоязычное видео в формате вопросов и ответов о раке (или просто опухолях), которое, вероятно, и не запомнилось бы мне, не будь там вопроса вроде «Почему бы не принимать лекарства от рака по аналогии с витаминами, чтобы его избежать?» ЛОЛ. Теперь читателю понятно, что использование таких препаратов на здоровом человеке как минимум ухудшит его здоровье, может вызывать рак, а передозировка попросту убьет, как убивает иприт.
Ну и ради интереса привожу формулы химиотерапевтических противоопухолевых препаратов в которых читатель с легкостью найдет основу азотистого иприта:
Урамустин, хлорэтиламиноурацил, урацил мустард, допан
Мелфалан «Алкеран», «Сарколизин»
Хлорамбуцил
Бендамустин
Манномустин, Дегранол
Преднимустин

Эстрамустин

Новэмбихин
Пафенцил
Лофенал
Циклофосфамид
Ифосфамид

Мафосфамид

Трофосфамид, Иксотен
Перфосфамид, Пергамид
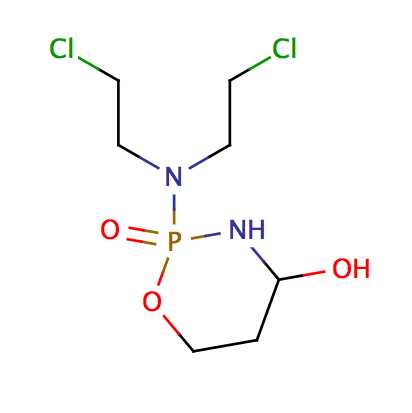
Гидроксициклофосфамид
Алдофосфамид
Глюфосфамид
И т.д.
Подводя итог сказанному можно задать вопрос, сколько людей погибло в результате применения иприта (на месте, от последствий, в процессе производства иприта, в процессе его утилизации и т.п.) и сколько получили дополнительные годы, иногда и десятилетия, в результате применения химиотерапевтических препаратов на основе иприта? Лично я уверен, что число вторых уже давным давно превысило число первых, так что в данном случае работает пословица «нет худа без добра». Скажем, не будь применения кожнонарывных ОВ во времена Первой мировой, использование противоопухолевых препаратов отодвинулось бы на несколько десятилетий вперед, может, еще на больший срок. Также произошло и с химией мышьяка — поиски новых ОВ на основе мышьяка дали мощный толчок химиотерапевтическим препаратам сифилиса (впрочем, химия мышьякорганических соединений развивалась еще в довоенный период).
habr.com
Иприт | Info-Farm.RU
Иприт, бис (2-хлороетил) сульфид — сульфуроорганична соединение состава (ClCH 2 CH 2)2 S. Иприт впервые был получен немецким химиком Виктором Меером в 1886 году. Этому предшествовали работы химиков Деспре (1822), Немана (1859), Гутмана (1860), которые исследовали данный класс соединений, однако не выделили ее в чистом виде.
Чистый иприт представляет собой бесцветную маслянистую веществом без запаха (технический иприт имеет чесночно-горчичный запах и желто-коричневый цвет). Плохо растворяется в воде и неограниченно — во многих органических растворителях.
Во времена Первой мировой войны иприт применялся как боевое отравляющее вещество кожно-нарывного действия. Международное обозначение иприта как химического оружия — HD. Боеприпасы с ипритом в Германии сказывались желтым крестом (он входит в состав боевой смеси желтый крест, нем. Gelbkreuz), в США кодируются двумя зелеными кольцами.
В 1993 году, в результате подписания Конвенции о химическом оружии, использование иприта как химического оружия было запрещено. Его включили в список 1, который регламентирует производство и оборот опасных веществ.
Срок иприт происходит от названия бельгийского города Ипр, вблизи которого в ночь на 13 июля 1917 немецкими войсками впервые применен данное вещество как химическое оружие.
Токсическое действие иприта заключается в повреждении глаз, кожи, дыхательных путей. Симптомы отравления проявляются со скрытым периодом в 2:00, но при жаркой погоде и влажной кожи они появляются сразу. Следствием контакта с веществом появление пузырьки с желтоватой жидкостью, которые долго заживают и оставляют рубцы. При концентрации иприта в воздухе 0,03 мг / л смерть наступает в течение 2-5 минут.
Вещество быстро проникает в строительные материалы, поглощается текстилем, резиной, бумагой, поэтому отравления возможно и при контакте с зараженными предметами.
Физические свойства
Чистый иприт представляет собой бесцветную маслянистую жидкость со слабым запахом касторки, технический продукт имеет цвет от желтого до темно-коричневого и резкий запах (чеснока или горчицы). Плотность паров по воздуху составляет 3,5. Давление пара при 20 ° С — 0,072 мм рт. ст.
Температура плавления чистого вещества составляет 14,5 ° C, а у технического иприта, вследствие наличия примесей, она несколько ниже. Для предотвращения замерзания во время Первой мировой войны в него добавляли хлоропикрин, хлоробензен, Тетрахлорметан.
Плохо растворяется в воде (менее 1%), неограниченно растворяется в маслах, жирах, бензине, керосине, ацетоне, Тетрахлорметан, спиртах, хлоропикрини. Смешивается с другими ядовитыми веществами: етилдихлороарсином, фенилдихлороарсином, люизитом.
Летучесть иприта: 75 мг / м³ при 0 ° C (твердый), 610 мг / м³ при 20 ° C (жидкий), 2 860 мг / м³ при 40 ° C (жидкий).
Не вызывает коррозии при хранении его в алюминиевых контейнерах; латунь быстро корродирует при температуре 65 ° C. Во влажном воздухе технический иприт с примесями, которые образуются в результате его разложения (сероводород, хлороводород, этилен), вызывает коррозию стали.
Получение
Существует три основных способа синтеза иприта: с оксиран (оксида этилена), этилена и винилхлорида.
Синтез с оксиран проводится при температуре 80 ° C в две стадии: сульфированием с помощью сероводорода или гидросульфидов для получения тиодигликолю, а впоследствии — хлорированием соединения:
После вакуумной дистилляции получают иприт с чистотой 95%. Выход синтеза составляет 90%. Этот способ впервые был проведен немецким химиком В. Меером в 1886 году.
Синтез иприта из этилена и хлоридов серы разрабатывался во времена Первой мировой войны, а после ее окончания. Преобладающим способом получения является реакция с SCl 2:
Хлорид серы (II) обычно имеет примеси дихлорополисульфидив (S 2 Cl 2, S 3 Cl 2, S 5 Cl 2), поэтому конечный продукт может быть загрязнен хлороетилполисульфидамы (ClCH 2 CH 2)2S x. Имеющийся в реакционной смеси свободный хлор может образовывать полихлорированные примеси.
Получение иприта с винилхлорида является наиболее целесообразным, учитывая легкость протекания реакции — она происходит уже при комнатной температуре (15-25 ° C):
Как инициаторы реакции используют органические перекиси и ультрафиолетовое излучение. Реакция в течение 10 минут с выходом продукта около 75%. При использовании вместо сероводорода 1-меркапто-2-хлороетану HSCH 2 CH 2 Cl выход реакции приближается к 100%.
Химические свойства
Иприт медленно гидролизуется с образованием соляной кислоты и тиодигликолю:
Он слабо растворяется в воде, поэтому может не испытывать гидролиза длительное время. Процесс гидролиза ускоряют повышение температуры и присутствие щелочей.
Одной из важнейших реакции является действие уротропина при гидролиза: продуктом взаимодействия создаваемой соляной кислоты с уротропином является формальдегид, который способствует заживлению ран:
При действии сильных окислителей (перманганата калия, хроматных кислоты, азотной кислоты, гипохлоритов), сульфид окисляется до сульфоксида, а затем — в сульфона:
Несмотря на то, что продукты окисления также являются ядовитыми веществами, этот способ применяется для дегазации, потому как они являются кристаллическими веществами и не оказывают воздействия на кожу.
Подобно другим тиоетерив, иприт способен образовывать с солями металлов сульфониеви соединения. Образуемые комплексы имеют характерную окраску, а иногда и низкую растворимость, поэтому иногда применяются в аналитической химии. Чаще реакция проводится с галогенидами тяжелых металлов: йодидами и хлоридами меди, цинка, титана, платины, ауру:
Токсичность
Иприт действует на организм человека или ингаляционная и контактный яд: капли и аэрозоли иприта поражают дыхательные пути, кожу, глаза.
Вещество способно проникать в организм через кожу. Эта способность зависит от температуры окружающей среды: при 21-23 ° C проникновения составляет 1,4 · 10 -3 мг / (см² · мин), при высоких — около 2,7 · 10 -3 мг / (см² · мин). Проникновение в организм иприта в количестве 6 · 10 -3 в половине случаев вызывает появление волдырей. Образование небольших эритем происходит при дозе 0,01 мг / см кожи, крупных — при дозе 0,5 мг / см. Глаза поражаются даже ипритом небольшой концентрации: его действие при концентрации 1,2 · 10 -3 мг / л в течение 45 минут вызывает воспаление глаз, спазмы век, светобоязнь, которые продолжаются до 4 недель.
Действие иприта концентрацией 0,03 мг / л в течение 2-5 минут является летальной. Концентрация 0,01 мг / л опасна в течение 15 минут и ведет к сильным повреждений глаз, кожи.
Контакт иприта за кожей первоначально не вызывает никаких неприятных ощущений. В течение первых 2-5 минут он проникает сквозь кожу, далее растворяется в подкожном жире и впоследствии, через 20-30 минут, полностью всасывается и попадает в кровь. После всасывания наступает скрытый период продолжительностью от 2:00 до суток в зависимости от дозы, температуры и влажности воздуха, структуры и влажности кожи. В жаркую погоду, при горячей, влажной кожи или нежных её участков период скрытого действия значительно сокращается и может быть почти отсутствующим.
Первые признаки поражения после окончания периода скрытого действия проявляются в виде зуда, жжения и покраснения кожи (эритемы) в местах контакта с жидким или газообразным ипритом. Кожа натягивается, становится сухой и теплой. При небольших дозах эти явления через несколько суток проходят. При более высоких дозах развивается отечность, по краям которой через 16-30 часов после контакта с ядом появляется множество мелких пузырьков. В дальнейшем они сливаются в большие или один большой пузырь с бесцветной или желтоватой жидкостью. Пузырьки прорываются и на коже образуются болезненные ипритни язвы, заживление которых может продолжаться более 2 месяцев. Вторичная инфекция может привести к гнойным воспалениям пораженных участков кожи. На их месте остаются рубцы.
Защита
Основной защитой от иприта, в частности, глаз, лица и дыхательных путей, является противогаз. После попадания на хлопчатобумажную одежду иприт за 3:00 полностью пропитывает его, что может в дальнейшем повлечь дополнительные поражения. Для предотвращения попадания соединения на одежду и под него, пользуются специальными защитными костюмами.
Для обработки кожи (устранение незначительных капель иприта), одежды или предметов, которые контактировали с ипритом, применяют окислители и агенты хлорирования (гипохлориты, хлорная известь, хлороамиды).
Изображения по теме
info-farm.ru
Смерть из пробирки (часть 2) » Военное обозрение
Продолжение. Предыдущая часть здесь: Смерть из пробирки (часть 1)
Думаю, пришло время подвести первые итоги.
Противостояние брони и снаряда — тема, такая же вечная, как и сама война. Химическое оружие — не исключение. За два года применения (1914—1916 гг.) оно уже успело эволюционировать от практически безвредных (насколько этот термин вообще применим в данном случае) лакриматоров
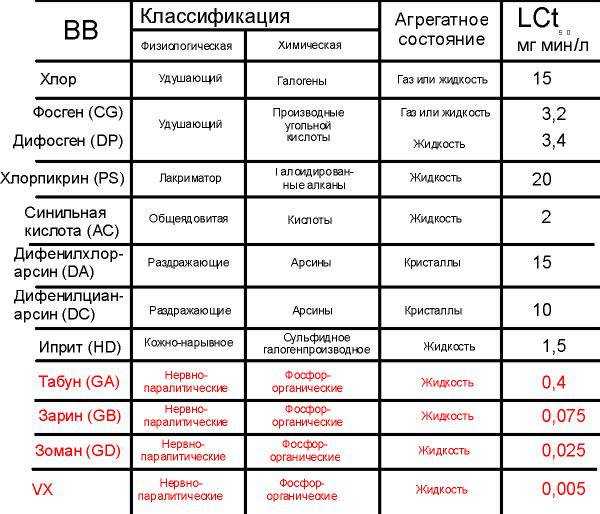
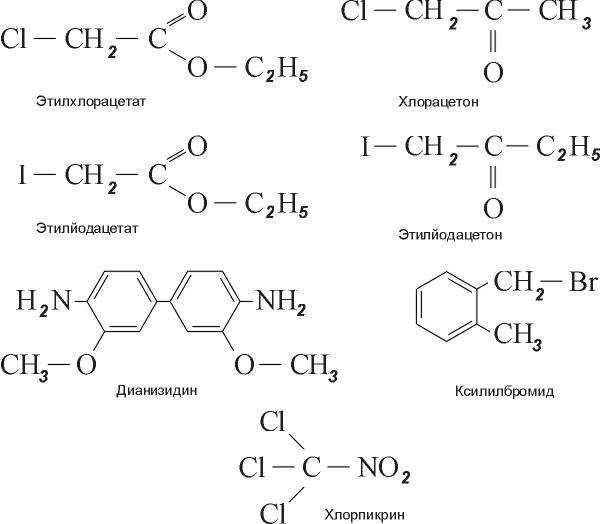 до убийственных ядов [3]:
до убийственных ядов [3]:Для наглядности они сведены в таблицу
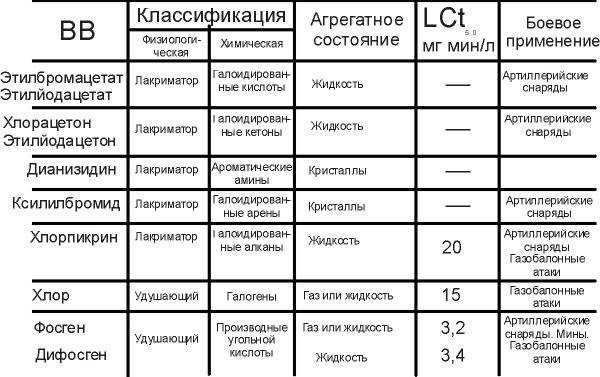
LCt50 — относительная токсичность ОВ [5]
Как видно, все представители первой волны ОВ были направлены на наиболее поражаемые органы человека (легкие) и не были рассчитаны на встречу со сколько-нибудь серьезными средствами защиты. Но изобретение и широкое применение противогаза внесло изменения в извечное противостояние брони и снаряда. Воющим странам вновь пришлось нанести визит в лаборатории, после чего в окопах явились производные мышьяка и серы.
Фильтры первых противогазов в качестве активного тела содержали только импрегнированный активированный уголь, что делало их очень эффективными против паро- и газообразных веществ, но они легко «пробивались» твердыми частицами и капельками аэрозоля. Отравляющими веществами второго поколения стали арсины и иприт.
Французы и здесь доказали, что они неплохие химики. 15 мая 1916 года во время артиллерийского обстрела они применили смесь фосгена с четыреххлористым оловом и треххлористым мышьяком (COCl2, SnCl4 и AsCl3), а 1 июля — смесь синильной кислоты с треххлористым мышьяком (HCN и AsCl3). Даже мне, дипломированному химику, с трудом удается представить себе тот филиал ада на земле, какой образовался после этой артподготовки. Правда, один нюанс не отметить нельзя: применение синильной кислоты в качестве ОВ — занятие совершенно бесперспективное, ибо, несмотря на свою славу записного убийцы, она — вещество чрезвычайно летучее и нестойкое. Но паника при этом возникла нешуточная — сия кислота не задерживалась ни одним противогазом того времени. (Справедливости ради необходимо сказать, что и нынешние противогазы с этой задачей справляются не очень хорошо — необходима специальная коробка.)
Немцы не стали долго тянуть с ответом. И он был намного более сокрушающим, ибо примененные ими арсины были гораздо более сильными и специализированными веществами.
Дифенилхлорарсин и дифенилцианарсин — а это были именно они — были не только гораздо смертоносней, но и из-за сильного «пробивного действия» получили название «вредителей противогазов». Снаряды с арсином маркировали «синим крестом».
Арсины — твердые вещества. Чтобы их распылять, потребовалось значительно усилить заряд взрывчатого вещества. Так на фронте вновь появился осколочно-химический снаряд, но уже чрезвычайно более мощный по своему действию. Дифенилхлорарсин был применен немцами 10 июля 1917 года в сочетании с фосгеном и дифосгеном. С 1918 года он был заменен дифенилцианарсином, но еще применялся как индивидуально, так и в смеси с преемником.
Германцами даже была выработана методика комбинированного огня снарядами «синего» и «зеленого креста». Снаряды «синего креста» поражали противника осколками и заставляли снимать противогазы, снаряды «зеленого креста» отравляли бойцов, снявших маски. Так зародилась новая тактика химической стрельбы, получившая красивое название «стрельбы разноцветным крестом».
Июль 1917 года оказался богат на дебюты немецких ОВ. Двенадцатого числа под тем же многострадальным бельгийским Ипром немцы применили новинку, ранее на фронтах не появлявшуюся. В этот день по позициям англо-французских войск было выпущено 60 тыс. снарядов, содержащих 125 т желтоватой маслянистой жидкости. Так Германией впервые был применён иприт.
Это ОВ было новинкой не только в химическом смысле — серные производные еще в этом качестве не использовались, но оно стало еще и родоначальником нового класса — кожно-нарывных ОВ, обладавший к тому же еще и общеядовитым действием. Свойства иприта проникать через пористые материалы и вызывать тяжелые поражения при контакте с кожей обусловили необходимость иметь защищающимся, помимо противогаза, защитную одежду и обувь. Снаряды, снаряженные ипритом, стали маркировать «желтым крестом».
Хотя иприт предназначался для «обхода» противогазов, в ту страшную ночь у британцев их не оказалось вообще — непростительная беспечность, последствия которой блекнут только на фоне ее несущественности.
Как это часто бывает, одна трагедия следует за другой. Вскоре британцы перебросили резервы, на этот раз в противогазах, но через несколько часов и они оказались отравленными. Будучи очень стойким на местности, иприт в течение нескольких дней отравлял войска, присылаемые командованием на смену пораженным с упорством, достойным лучшего применения. Потери британцев были столь велики, что наступление на этом участке пришлось отложить на три недели. По оценкам германских военных, ипритные снаряды оказались примерно в 8 раз эффективнее для поражения личного состава войск противника, чем их же снаряды «зеленого креста».
К счастью для союзников, в июле 1917 года германская армия еще не располагала ни большим количеством ипритных снарядов, ни защитной одеждой, которая позволила бы осуществить наступление на местности, зараженной ипритом. Однако по мере того как германская военная промышленность наращивала темпы производства ипритных снарядов, ситуация на Западном фронте стала приобретать для союзников далеко не лучший вид. Внезапные ночные обстрелы позиций британских и французских войск снарядами «желтого креста» стали повторяться все чаще. Количество отравленных ипритом в войсках союзников росло. Всего за три недели (с 14 июля по 4 августа включительно) англичане потеряли только от иприта 14 726 человек (из них умерших — 500). Новое отравляющее вещество серьезно мешало работе британской артиллерии, немцы легко брали верх в контрорудийной борьбе. Зараженными ипритом оказывались районы, намечаемые для сосредоточения войск. Вскоре появились и оперативные последствия его применения. В августе-сентябре 1917 года иприт заставил захлебнуться наступление 2-й французской армии под Верденом. Французские атаки по обоим берегам Мааса были отражены немцами посредством снарядов «желтого креста».
По мнению многих германских военных авторов 1920-х гг., союзникам не удалось осуществить планируемый на осень 1917 года прорыв германского фронта именно из-за широкого применения германской армией снарядов «желтого» и «разноцветного» крестов. В декабре германская армия получила новые инструкции для применения химических снарядов разных типов. С присущей немцам педантичностью каждому типу химических снарядов давалось строго определенное тактическое назначение и указывались приемы применения. Инструкции еще окажут очень плохую услугу самому германскому командованию. Но это произойдет позже. А пока немцы были полны надежд! Они не дали «перемолоть» свою армию в 1917 году, Россия вышла из войны, благодаря чему немцы впервые добились небольшого численного перевеса на Западном фронте. Теперь им надо было достичь победы над союзниками до того, как американская армия станет реальным участником войны.
Эффективность иприта стала настолько большой, что его применяли практически повсеместно. Он тек по улицам городов, заполнял луга и лощины, отравлял реки и озера. Участки, зараженные ипритом, на картах всех армий обозначались желтым цветом (эта маркировка участков местности, пораженных ОВ любого типа, осталась и поныне). Если хлор стал ужасом Первой мировой войны, то иприт, без сомнения, может претендовать на роль ее визитной карточки. Стоит ли удивляться, что германское командование стало рассматривать химическое оружие как главную гирю на весах войны, которую оно собиралось использовать, чтобы склонить чашу победы на свою сторону (ничего не напоминает, а?). Германские химические заводы ежемесячно выпускали свыше тысячи тонн иприта. При подготовке большого наступления в марте 1918 года германская промышленность наладила выпуск 150-мм химического снаряда. Он отличался от предыдущих образцов сильным зарядом тротила в носовой части снаряда, отделенного от иприта промежуточным днищем, что позволяло более эффективно распылять ОВ. Всего было произведено более двух миллионов (!) снарядов с ОВ разного типа, которые были использованы в ходе операции «Михаэль» в марте 1918 года. Прорыв фронта на участке Левен — Гузокур, наступление на реке Лис во Фландрии, штурм горы Кеммель, сражение на реке Эн, наступление на Компьен — все эти успехи, среди прочего, стали возможными благодаря и применению «разноцветного креста». Об интенсивности применения ОВ говорят хотя бы такие факты.
9 апреля ураганному обстрелу «разноцветным крестом» подверглась полоса наступления. Обстрел Армантьера оказался настолько действенным, что иприт буквально затопил его улицы. Англичане без боя покинули отравленный город, однако и сами германцы смогли войти в него только через две недели. Потери англичан в этом сражении отравленными достигли 7 тыс. человек.В полосе наступления на гору Кеммель германская артиллерия выпустила большое количество снарядов «синего креста» и в меньшем количестве снаряды «зеленого креста». В тылу противника было установлено заграждение «желтым крестом» от Шеренберга до Крюстстрааетсхука. После того как британцы и французы, спешившие на помощь гарнизону горы Кеммель, наткнулись на участки местности, зараженные ипритом, они прекратили всякие попытки выручить гарнизон. Потери англичан с 20-го по 27 апреля — около 8500 человек отравленных.
Но время побед для германцев истекало. Американские подкрепления все в большем количестве прибывали на фронт и с энтузиазмом вступали в бой. Союзники широко применяли танки и авиацию. Да и в деле самой химической войны они многое переняли у немцев. К 1918 г. химическая дисциплина их войск и средства защиты от отравляющих веществ уже превосходили германские. Была подорвана и германская монополия на иприт. Освоить довольно сложный синтез Майера-Фишера союзники не смогли, поэтому производили иприт по более простому методу Ниемана или Попе-Грина. Их иприт был менее качественным, содержал большое количество серы и плохо хранился, но кто собирался запасать его впрок? Производство его стремительно нарастало как во Франции, так и в Англии.
Немцы боялись иприта не меньше, чем их противники. Паника и ужас, вызванные применением французами 13 июля 1918 года ипритных снарядов против 2-й Баварской дивизии, стали причиной поспешного отхода всего корпуса. 3 сентября англичане начали использование на фронте собственные ипритные снарядов с таким же опустошительным эффектом. Сыграла злую шутку и немецкая педантичность в применении ОВ. Категорическое требование германских инструкций применять для обстрела пункта атаки только снаряды с нестойкими отравляющими веществами, а для прикрытия флангов — снаряды «желтого креста», привело к тому, что союзники в период германской химической подготовки по распределению по фронту и в глубину снарядов со стойкими и малостойкими отравляющими веществами точно выясняли, какие участки, предназначены противником для прорыва, а также предполагаемую глубину развития каждого из прорывов. Длительная артиллерийская подготовка давала в руки союзного командования ясную схему германского плана и исключала одно из главных условий успеха — внезапность. Соответственно, принятые союзниками меры в значительной степени снижали последующие успехи грандиозных химических атак германцев. Выигрывая в оперативном масштабе, немцы ни одним из своих «больших наступлений» 1918 года не достигали поставленных стратегических целей.
После провала германского наступления на Марне союзники захватили инициативу на поле боя. В том числе и в плане применения химического оружия. Что было дальше, известно всем…
Но будет ошибкой думать, что история «боевой химии» на этом закончилась. Как известно, что-либо однажды примененное, будет долго будоражить умы генералов. А с подписанием мирных договоров война, как правило, не заканчивается. Просто она переходит в другие формы. И места. Прошло совсем немного времени, и из лабораторий пришла новая генерация смертоносных веществ —фосфорорганические ОВ.
После окончания Первой мировой войны химическое оружие заняло прочное, и далеко не последнее место в арсеналах воевавших стран. В начале 30-х годов мало кто сомневался, что новая схватка ведущих держав не обойдется без широкомасштабного применения химического оружия.
По итогам Первой мировой войны лидером среди отравляющих веществ стал действующий в обход противогаза иприт. Поэтому исследования по созданию нового химического оружия велись в направлении совершенствования ОВ кожно-нарывного действия и средств их применения. С целью поиска более токсичных аналогов иприта в период между мировыми войнами были синтезированы сотни структурно-родственных соединений, но ни одно из них по совокупности свойств не обладало преимуществом перед «старым добрым» ипритом времен Первой мировой войны. Недостатки отдельных ОВ компенсировали созданием рецептур, то есть получением смесей ОВ с различными физико-химическими и поражающими свойствами.
К наиболее «видным» представителям межвоенного периода развития смертоносных молекул следует отнести люизит — кожно-нарывное ОВ класса хлорированных арсинов. Кроме основного действия, он также поражает сердечно-сосудистую, нервную систему, органы дыхания, желудочно-кишечный тракт.
Но никакие совершенствования рецептур или синтез новых аналогов ОВ, проверенных на поле боя в годы Первой мировой войны, не выходили за рамки общего уровня знаний того времени. Судя по противохимическим руководствам 1930-х годов, способы их применения и средства защиты были достаточно очевидными.
В Германии исследования по военной химии были запрещены Версальским договором, и инспектора союзников внимательно следили за его соблюдением. Поэтому в немецких химических лабораториях изучались лишь химические соединения, предназначенные для борьбы с насекомыми и сорняками — инсектициды и гербициды. Среди них была группа соединений производных кислот фосфора, которые химики изучали уже почти 100 лет, поначалу даже не подозревая о токсичности некоторых из них для людей. Но в 1934 году сотрудник германского концерна «ИГ-Фарбенидустри» Герхард Шредер синтезировал новый инсектицид табун, оказавшийся при вдыхании почти в 10 раз более токсичным, чем фосген, и способный вызвать смерть человека в течение нескольких минут при явлениях удушья и судорог, переходящих в паралич.
Как оказалось, табун (в системе обозначений он получил маркировку GA) представлял принципиально новый класс боевых ОВ, обладающих нервно-паралитическим действием. Вторым новшеством было то, что механизм действия нового ОВ был достаточно понятен: блокирование нервных импульсов со всеми вытекающими из этого последствиями. Было очевидно и другое: за свою смертоносность отвечает не вся молекула в целом или один из ее атомов (как это было ранее), а специфическая группировка, несущая в себе вполне определенное химико-биологическое действие.
Немцы всегда были отличными химиками. Полученные теоретические представления (пусть еще и не такие полные, как мы имеем в настоящее время) позволили вести целенаправленный поиск новых смертоносных веществ. Уже непосредственно перед войной германские химики под руководством Шредера синтезировали зарин (GB, 1939 г.) и, уже в ходе войны, зоман (GD, 1944 г.) и циклозарин (GF). Все четыре вещества получили обобщающее название «G-серия». Германия вновь получила качественное преимущество перед своими противниками в области химических вооружений.
Все три ОВ — прозрачные, похожие на воду жидкости; при незначительном нагревании легко испаряются. В чистом виде практически не имеют запаха (табун имеет слабый приятный запах фруктов), поэтому при высоких его концентрациях, легко создаваемых в полевых условиях, внутри организма может быстро и незаметно накопиться смертельная доза.
Прекрасно растворяются не только в воде, но и во многих органических растворителях, имеют стойкость от нескольких часов до двух суток, быстро впитываются в пористые поверхности (обувь, ткань) и кожу. Даже в настоящее время такое сочетание боевых возможностей оказывает завораживающее влияние на воображение генералов и политиков. То, что применять новые разработки на полях новой мировой войны не пришлось — величайшая историческая справедливость, ибо можно только догадываться, какой мелкой могла бы показаться минувшая мировая бойня в случае применения соединений «элемента мысли».
То, что применить Германии новые ОВ в ходе новой войны не дали, вовсе не означало, что работы над ними не будут продолжены. Захваченные запасы ФОВ (а счет их шел на тысячи тонн) были тщательно изучены и рекомендованы к применению и модификации. В 50-х годах появилась новая серия нервно-паралитических ОВ, которые в десятки раз токсичнее других ОВ такого же действия. Они получили маркировку V-газы. Пожалуй, каждый выпускник советской школы на уроках НВП в теме «Химическое оружие и защита от него» слышал аббревиатуру VX. Это — пожалуй, самое токсичное из искусственно созданных веществ, которое, к тому же, еще и массово производилось химическими комбинатами планеты. Химически он называется S-2-диизопропиламиноэтиловый или О-этиловый эфир метилтиофосфоновой кислоты, но правильнее его будет называть Концентрированной Смертью. Только из любви к химии помещаю портрет этого смертоносного вещества:
Даже в школьном курсе говорят, что химия — наука точная. Поддерживая это реноме, предлагаю сравнить значения токсичности этих представителей нового поколения убийц (ОВ подобраны в порядке, приблизительно соответствующем хронологии их применения или появления в арсеналах):
Ниже приведена диаграмма, иллюстрирующая изменение токсичности приведенных ОВ (по оси ординат отложена величина -lg(LCt50), как характеристика степени возрастания токсичности). Довольно наглядно видно, что период «проб и ошибок» закончился довольно быстро и с применение арсинов и иприта поиск эффективных ОВ велся в направлении усиления поражающего действия, что особенно ярко продемонстрировала серия ФОВ.

В одном из своих монологов М. Жванецкий сказал: «Что с человеком ни делай, он упорно ползет на кладбище». Можно спорить по поводу осознанности и желания этого процесса каждым отдельным человеком, но в том, что мечтающие о мировом господстве политики и лелеющие эти мечты генералы готовы ради достижения своих целей отправить туда добрую половину человечества, сомневаться не приходится. При этом они, разумеется, себя в этой части не видят. А вот отраве безразлично, кого убивать: противника или союзника, своего или чужого. Да и выполнив свою черную работу, она не всегда будет стремиться покинуть поле боя. Вот дабы не попасть под собственные «гостинцы», как англичане в ПМВ, появилась «гениальная» идея: снаряжать боеприпасы не готовым ОВ, а только его компонентами, которые при смешении могут относительно быстро прореагировать друг с другом, образуя смертоносное облако.
Химическая кинетика говорит, что наиболее быстро реакции будут протекать при минимальном количестве реагирующих веществ. Так на свет появились бинарные ОВ. Таким образом, химическому боеприпасу придается дополнительная функция химического реактора.
Такая концепция не является суперновым открытием. Она изучалась в США перед началом и в годы ВМВ. Но активно этим вопросом начали заниматься только во второй половине 50-х годов. В 60-х годах арсеналы ВВС США пополнились бомбами с зарядом VX-2 и GB-2. Двойка в обозначении указывает на число компонентов, а буквенная маркировка — на то вещество, которое появляется в результате их смешивания. Кроме того, в состав компонентов могут входит небольшие количества веществ-катализаторов и активаторов реакции.
Но, как известно, за все приходится платить. Удобство и безопасность бинарных боеприпасов куплены за счет меньшего количества ОВ по сравнению с такими же унитарными: место «съедают» перегородки и устройства для перемешивания реагентов (в случае необходимости). Кроме того, будучи веществами органической природы, взаимодействуют они достаточно медленно и не полностью (практический выход реакции около 70-80%). В сумме это дает приблизительно потерю эффективности в 30-35%, что должно компенсироваться большим расходом боеприпасов. Все это, по мнению многих военных специалистов, говорит о необходимости дальнейшего совершенствования систем бинарного вооружения. Хотя, как кажется, куда уже дальше, когда и так перед ногами бездонная могила…
Даже такой относительно небольшой экскурс в историю химического оружия позволяет сделать вполне определенный вывод.
Химическое оружие было изобретено и впервые применено не «восточными деспотиями» типа России, а самыми что ни на есть «цивилизованными странами», ныне носителями «высочайших стандартов свободы, демократии и прав человека» — Германией, Францией и Соединенным Королевством. Будучи вовлеченной в химическую гонку, Россия не стремилась создавать новые яды, в то время как ее лучшие сыны тратили свое время и энергию на создание эффективного противогаза, конструкцией которого поделились с союзниками.
Советской власти в наследство досталось все, что хранилось на складах российской армии: около 400 тыс. химических снарядов, десятки тысяч баллонов со специальной арматурой для газопусков хлоро-фосгеновой смеси, тысячи огнеметов разных типов, миллионы противогазов Зелинского-Кумманта. Также сюда следует отнести более десятка фосгеновых заводов и цехов и первоклассно оборудованные лаборатории по противогазовому делу Всероссийского земского союза.
Новая власть прекрасно понимала, с какими хищниками ей придется иметь дело, и меньше всего желала повторения трагедии 31 мая 1915 г. под Болимовом, когда русские войска оказались беззащитными перед химическим нападением германцев. Ведущие химики страны продолжили свои работы, но не столько по усовершенствованию орудий уничтожения, сколько по созданию новых средств защиты от него. Уже 13 ноября 1918 г. приказом Реввоенсовета Республики № 220 была создана Химическая служба РККА. Тогда же были созданы Всероссийские советские курсы военной газотехники, где готовили военных химиков. Можно сказать, что начало славной истории советских (а теперь российских) войск радиационной, химической и биологической защиты была положено именно в те грозные и неспокойные годы.
В 1920 г. курсы преобразовали в Высшую военно-химическую школу. В 1928 г. в Москве была создана научно-исследовательская организация в области химического оружия и средств противохимической защиты — Институт химической обороны (в 1961 г. переведен в г. Шиханы), а в мае 1932 г. сформирована Военно-химическая академия для подготовки специалистов-химиков для РККА.
За двадцать послевоенных лет в СССР были созданы все необходимые системы вооружения и средства поражения, которые позволяли надеяться на достойный ответ противнику, рискнувшему их применить. И в послевоенное время войска химической защиты готовы были использовать все имеющиеся в их арсенале силы и средства для адекватной реакции на любую сложившуюся обстановку.
Но… Судьба столь «перспективного» средства массового убийства людей сложилась парадоксально. Химическому оружию, также как впоследствии и атомному, было суждено превратиться из боевого в психологическое. И пусть все так и остаётся. Хочется верить, что потомки учтут опыт предшественников и не повторят их смертоносных ошибок.
Как говорил Марк Твен, в любом писательском труде самое трудное — это поставить последнюю точку, так как всегда остается еще что-то, о чем хотелось бы рассказать. Как я и подозревал с самого начала, тема оказалась столь же обширной, сколь и трагичной. Поэтому позволю себе завершить свой небольшой химико-исторический обзор разделом под названием «Историческая справка или картинная галерея убийц».
В этой части будут приведены краткие сведения об истории открытия всех участником нашего исследования, которых, будь они живыми людьми, можно было бы смело причислять к списку самых опасных массовых убийц.
Хлор. Первое искусственно созданное соединение хлора — хлороводород — было получено Джозефом Пристли в 1772 г. Элементарный хлор был получен в 1774 г. шведским химиком Карлом Вильгельмом Шееле, описавшим его выделение при взаимодействии пиролюзита (диоксида марганца) с соляной кислотой (раствором хлороводорода в воде) в своём трактате о пиролюзите.
Бром. Был открыт в 1826 году молодым преподавателем колледжа города Монпелье Антуаном Жеромом Баларом. Открытие Балара сделало его имя известным всему миру, несмотря на то, что он был весьма заурядным преподавателем и довольно посредственным химиком. С его открытием связан один курьез. Небольшое количество брома в прямом смысле «держал в руках» Юстус Либих, но посчитал его одним из соединений хлора с йодом и исследования забросил. Такое пренебрежение к науке, впрочем, не помешало ему потом ехидно сказать: «Это не Балар открыл бром, а бром открыл Балара». Ну, как говорится, каждому свое.
Синильная кислота. Широко представлена в природе, содержится в некоторых растениях, коксовом газе, табачном дыме (к счастью, в следовых, нетоксичных количествах). В чистом виде получена шведским химиком Карлом Вильгельмом Шееле в 1782 году. Считается, что она стала одним из факторов, сокративших жизнь великому химику и ставшим причиной тяжелого отравления и смерти. Позднее была исследована Гитоном де Морво, предложившим способ получения ее в товарных количествах.
Хлорциан. Получен в 1915 году Жозефом Луи Гей-Люссааком. Он же получил и дициан — газ, являющийся родоначальником как синильной кислоты, так и многих других цианистых соединений.
Этилбром(йод)ацетат. Достоверно установить, кто именно первым получил сии представители славного рода отравителей (а скорее, слезоточителей), возможности не представилось. Скорее всего, они явились побочными детьми открытия в 1839 году Жаном Батистом Дюма хлорпроизводных уксусной кислоты (из личного опыта замечу — действительно, вонючка ещё та).
Хлор(бром)ацетон. Обе едкие вонючки (тоже личный опыт, увы) получаются аналогичными способами по методу Фрича (первый) или Штолля (второй) прямым действием галогенов на ацетон. Получены в 1840-х годах (более точной даты установить не удалось).
Фосген. Получен Гемфри Деви в 1812 году при облучении ультрафиолетовым светом смеси угарного газа и хлора, за что и получил столь возвышенное имя — «рожденный светом».
Дифосген. Синтезирован французским химиком Огюстом-Андре-Тома Кауром в 1847 году из пентахлорида фосфора и муравьиной кислоты. Кроме того, исследовал состав какодила (диметиларсина), в 1854 году он синтезировал триметиларсин и тетраметиларсоний, сыгравших не последнюю роль в химической войне. Впрочем, любовь французов к мышьяку вполне традиционна, я бы даже сказал — пламенна и нежна.
Хлорпикрин. Получен Джоном Стенхаузом в 1848 году как побочный продукт при исследовании пикриновой кислоты действием на последнюю хлорной известью. Он же дал ему и название. Как видим, исходные вещества вполне доступны (о ПК я уже писал несколько ранее), технология вообще проще не бывает (никаких нагреваний-перегонок-экстракций), поэтому этот способ практически без каких-либо изменений был применен в промышленных масштабах.
Дифенилхлорарсин (DA). Открыт немецким химиком Леонором Михаэлисом и французом Ла Костом в 1890 году.
Дифенилцианарин (DC). Аналог (DA), но открыт несколько позже — в 1918 году итальянцами Стурниоло и Беллицони. Оба отравителя почти аналоги и стали родоначальниками целого семейства ОВ на основе органических соединений мышьяка (прямые потомки арсинов Каура).
Иприт (HD). Эта визитная карточка Первой мировой впервые была синтезирована (ирония судьбы) бельгийцем по происхождению Сезаром Депре в 1822 году во Франции и в 1860 году независимо от него и друг от друга шотландским физиком и химиком Фредериком Гутри и бывшим немецким аптекарем Альбертом Ниманом. Все они исходили, как это ни странно, из одного и того же набора: дихлорида серы и этилена. Такое впечатление, что дьявол заранее позаботился о массовых поставках в грядущие годы…
История открытия (хвала небесам, не применения!) фосфорорганики описана выше. Так что повторяться нет необходимости.
Литература
1. http://xlegio.ru/throwing-machines/antiquity/greek-fire-archimedes-mirrors/.
2. http://supotnitskiy.ru/stat/stat72.htm.
3. http://supotnitskiy.ru/book/book5_prilogenie12.htm.
4. З. Франке. Химия отравляющих веществ. В 2-х т. Перевод с нем. М.: Химия, 1973.
5. Александров В.Н., Емельянов В.И. Отравляющие вещества: Учебн. пособие. М.: Воениздат, 1990.
6. Де-Лазари А.Н. Химическое оружие на фронтах мировой войны 1914-1918 гг. Краткий исторический очерк.
7. Антонов Н. Химическое оружие на рубеже двух столетий.
topwar.ru
1917 год — впервые на поле боя применен иприт — EADaily
12 июля 1917 года, у бельгийского города Ипр англо-французские войска были обстреляны немецкими минами, содержавшими маслянистую жидкость. Так, впервые Германией было совершено боевое применение иприта. В результате этой химатаки 87 военнослужащих стран Антанты погибли, еще 2490 получили поражения различной тяжести.
Первая мировая война после довольно динамичного начала быстро превратилась в «окопное» противостояние. На Западном фронте противоборствующие армии зарылись в землю, ощетинились минными полями и проволочными заграждениями. Наступательные операции стали совершенно неэффективными и обе стороны оказались в патовой ситуации. В результате, для прорыва обороны противника стали применять химическое оружие.
Применение ядовитых газов в Первой мировой войне было крупной военной инновацией. Диапазон действия отравляющих веществ шёл от просто вредоносных (таких, как слезоточивый газ) до смертельно ядовитых, как хлор и фосген. Химическое оружие является одним из основных в Первой мировой войне и в общей сложности на всём протяжении XX века. Смертельный потенциал газа был ограничен — лишь 4% смертей от общего количества поражённых. Тем не менее, доля смертельных случаев была высокой, а газ оставался одной из главных опасностей для солдат. Впоследствии появились средства защиты от газовых атак, в связи с чем, на более поздних этапах войны стала снижаться эффективность его использования, и он почти вышел из оборота.
Химическое оружие стало применяться с самого первого дня Первой мировой войны. Вопреки расхожему убеждению пионерами химических атак стали вовсе не немцы, а французы, которые в августе 1914 года применили против немецких солдат гранаты со слезоточивым газом (этилбромацетат). Однако запасы этилбромацетата у союзников быстро подошли к концу.
Первым же смертельным газом, использованным немецкими военными, был хлор — побочный продукт от производства красителей. 22 апреля 1915 года немецкая армия распылила 168 тонн хлора около реки Ипр. После битвы на Ипре отравляющие газы были применены Германией ещё несколько раз: 24 апреля против 1-й канадской дивизии, 2 мая около «Фермы-мышеловки», 5 мая против британцев и 6 августа против защитников русской крепости Осовец.
Иприт же был первым отравляющим газом, созданным специально для убийства людей — это жидкий отравляющий горчичный газ кожно-нарывного действия. Иприт обладает отчетливо выраженным местным действием — он поражает глаза и органы дыхания, желудочно-кишечный тракт и кожные покровы. Всасываясь в кровь, он проявляет и общеядовитое действие. Иприт поражает кожные покровы при воздействии, как в капельном, так и в парообразном состоянии. От капель и паров иприта обычное летнее и зимнее армейское обмундирование не защищает кожные покровы, как и практически любые виды гражданской одежды.
Первое применение иприта состоялось в ночь с 12 на 13 июля 1917 года под все тем же многострадальным городом Ипр, который и дал название газу. Поражения различной тяжести получили 2490 человек, из которых 87 скончались.
Ради справедливости стоит сказать, что под самый конец войны иприт успели применить и британцы. В Англии быстро расшифровали его формулу, но наладить производство нового отравляющего вещества удалось лишь в 1918 году, из-за чего использовать иприт в военных целях удалось лишь в сентябре 1918 года (за 2 месяца до перемирия).
eadaily.com
Химия войны | BroDude.ru

В разные времена людей убивали различными способами. Когда-то было достаточно заостренного камня, подобранного в соседней пещере, чтобы проломить голову незадачливому соседу, посмотревшему на твое имущество. Позже люди научились делать мечи и копья, строить катапульты или со стен крепостей поливать кипящим маслом головы неприятелей. Неожиданно белый человек получил огнестрельное оружие в руки и сразу же стер с лица земли целую цивилизацию майя, которая, в свою очередь, сама любила умерщвлять людей, закалывая их на жертвенных алтарях своих храмов. Вроде бы ружья, автоматы, и всевозможные пушки положили конец изощренным экспериментам с оружием, ведь что может быть действеннее пули? Да и пуля, как ни посмотри, гуманнее того, что было до нее. Но в период Первой мировой войны на человечество свалилась очередная опасность, имя которой — химия. Научную дисциплину взяли в оборот, рассчитывая получить оружие, от которого люди не просто гибнут, а перед этим еще и страдают от жутких последствий его применения.
Полководцы прошлого считали, что химическое оружие способно помочь выиграть битву малой кровью, не задействовав основные силы. Суть такого вида оружия была еще и в том, чтобы деморализовать противника, посредством вида ужасающих страданий, которое приносит то или иное вещество.
Фосген
Говорят, что фосген пахнет прелыми фруктами и сеном. Ну запах хоть и относительно приятный, а вот смерть от фосгена приятной точно не назовешь. Лавры за создание этого химического оружия мы отдаем английскому физику и химику Дэви Гемфри. Боевое состояние — бесцветный пар, который в 3,5 раза тяжелее воздуха. Данное вещество обладает большой летучестью, даже при низких температурах. Определить наличие фосгена в воздухе просто. Возьми тампон у подруги, смочи его раствором аммиака, и если тампон начнет выделять белый дым, то из квартиры лучше выйти, иначе будет отравление.
 Данное вещество начали активно применять на войне 1914-1918 годов.
Данное вещество начали активно применять на войне 1914-1918 годов.В основном его скидывали в окопы и траншеи врага, так стойкость пара увеличивалась до 3 часов вместо 30-50 минут на открытой местности. Ядовитым он является после вдыхания паров, причем признаки отравления проступают не сразу, а после скрытого периода, который протекает от 4 до 8 часов. Технически фосген вызывает быстро прогрессирующий отек легких (который чаще всего заканчивается смертью), нарушает проницаемость альвеол, и впоследствии ведет к удушению. Неприятный сладковатый привкус во рту, легкое головокружение, слезоточивость перерастают в нечто большее.
Начинается сильное давление на грудную клетку, ведь ритм частоты дыхания увеличивается от нормального показателя в 18-20 до критического — 40-70 в минуту. В более тяжелых случаях жертву этого ядовитого пара настигает нервно-психическое расстройство (галлюцинации, оглушение, аффективные нарушения). К сожалению, антидота против данного химического оружия не существует. Но если у тебя есть хороший противогаз, то ты в безопасности.
Иприт

К созданию иприта причастны сразу несколько видных ученых своего времени. Кто именно синтезировал иприт? Вопрос не так прост, как кажется. Можно лишь сказать, что Альберт Ниман сделал это первым в Германии, во Франции иприт был синтезирован Сезаром Депре, а в Британии — Фредериком Гутри.
Наибольшую известность это вещество получило в ночь с 12 по 13 июля 1917 года, когда немецкие войска применили Lost (изначально иприт был известен под таким промышленным названием) у бельгийского города Ипр. В результате этой битвы от химикатов погибло 5000 человек, еще 10000 получили травмы различной тяжести. Сама битва ознаменовала собой масштабное применение химического оружия на войне. Не только со стороны немцев, но и со стороны союзнических войск. Марлевые повязки в момент были заменены на противогазы. Преимущество иприта заключалось в том, что он мог проникать через обувь, обмундирование, и поражать кожу, даже в небольших количествах.
Чаще всего иприт применяли в качестве вещества сдерживающего, оборонительного. Более 80 % всех отравлений в период Первой мировой войны приходились на иприт. В основном поражению подвергались слизистые оболочки глаз, носоглотки, верхних дыхательных путей. Смерть от удушья могла наступить на 3-4 день. Если концентрация вещества была более высокой, то происходило общее отравление организма. Наверняка ты видел архивные фотографии времен войны, где на телах солдат красовались отвратительные язвы — это последствия воздействия иприта. Причем первые симптомы выглядят довольно невинно — простые покраснения, которые проявляются через 2-6 часов после воздействия вещества на организм. Но через сутки образуются небольшие пузыри, наполненные желтой жидкостью. Эти пузыри сливаются вместе, лопаются и образуют язву, которая не заживает на протяжении месяца, в лучшем случае.
Синильная кислота
Впервые на поле боя синильная кислота была использована французами 1 июля 1916 года, на реке Сомме. Однако в качестве оружия синильная кислота использовалась недолго. Причина в том, что на открытой местности этот яд очень быстро улетучивается, да и направлять его крайне сложно, в отличии от иприта.
 В целом, достаточно было подождать 10-15 минут, чтобы пространство вновь стало безопасным. Если речь идет о закрытом участке, то для того, чтобы избавиться от пагубного воздействия синильной кислоты, нужно было просто открыть окна и проветрить помещение. Впрочем, это вещество все равно внесло свою лепту в кровавое дело войны и использовалось впоследствии для куда более изощренных убийств. К примеру, синильная кислота применялась для исполнения смертных приговоров в США вплоть до 1999 года.
В целом, достаточно было подождать 10-15 минут, чтобы пространство вновь стало безопасным. Если речь идет о закрытом участке, то для того, чтобы избавиться от пагубного воздействия синильной кислоты, нужно было просто открыть окна и проветрить помещение. Впрочем, это вещество все равно внесло свою лепту в кровавое дело войны и использовалось впоследствии для куда более изощренных убийств. К примеру, синильная кислота применялась для исполнения смертных приговоров в США вплоть до 1999 года.Чаще всего кислота проникает в организм через дыхательные пути, но возможно поражение и через кожу, только при очень длительном воздействии и высокой концентрации. Сначала ты почувствуешь металлический привкус и жжение во рту, язык начнет неметь, глаза неприятно покалывать, а горло першить. Нервы натянутся как струны и ты ощутишь слабость, а после — головокружение. От неприятных ощущений возникнет чувство страха, дыхание станет неравномерным.
В конечном итоге ты потеряешь сознание и твое тело начнет испытывать судороги, за которыми наступает паралич, остановка дыхания, и ты уже труп. Но все может пройти гораздо быстрее, если концентрация синильной кислоты будет еще больше. Тогда сразу потеряешь сознание, впадешь в паралич и отправишься в небытие. Кстати, пахнет эта отрава горьким миндалем.
Agent оrange

Так называлось целое соединение из дефолиантов и гербицидов синтетического происхождения. Применялась эта гремучая смесь британской армией в Малайе и армией янки во Вьетнамской войне с 1961 по 1971 годы. Последние использовали этот вид химического оружия с воодушевлением ребенка, которому подарили целую коробку вкусных конфет. Не будем давать моральную оценку действиям американских войск, а просто расскажем о сути ада, происходящего с одной маленькой страной, где было слишком много лесов и слишком много партизан.
В общей сложности за весь период войны во Вьетнаме американские войска распылили 72 миллиона литров дефолиантов «Agent оrange». Это делали для уничтожения лесов, чтобы пустить кровь сопротивлению, которое сидело в зарослях и прятало там оружие. Но нередко данный химикат распылялся перед бомбардировкой населенных пунктов. Сам диоксид приводит к заболеваниям крови, печени, может вызвать рак и генетические мутации. В общей сложности 14 % от всей территории страны, подверглось воздействию этого яда. Вьетнамское «Общество пострадавших от диоксина» имеет свою суровую и печальную статистику: 3 миллиона пострадавших от диоксида, около миллиона человек в возрасте до 18 лет стали инвалидами или страдающими генетическими заболеваниями.
brodude.ru
Получение А) Иприта — Справочник химика 21
Выделяющаяся сера реагирует с дихлордиэтилсульфидом, образуя полисульфиды. Этот способ получения иприта использовался странами Антанты в первую мировую войну. В Германии иприт производили из тиогликоля (гл. 19, стр. 367). [c.194]Этилен служит, в частности, исходным продуктом при получении иприта [(С1—СНз—СНг) 2S]. Последний представляет собой бесцветную жидкость со слабым характерным запахом, малорастворимую в воде (0,8 г/л). В мировую войну 1914— 1918 гг. он применялся в качестве боевого отравляющего вещества, относящегося к классу стойких , т. е. заражающих местность на более или менее долгое время. Иприт вызывает воспаление кожи и образование трудно заживающих язв. [c.550]
Иприт может быть получен действием этилена на однохлористую серу [c.184]
Иприт впервые был получен в 1886 г. И. Д. Зелинским. [c.184]
Щие классификацию и измельчение крупных фракций, обеспечивающие получение порошкообразного продукта с дисперсным составом, близким к составу товарного ПВХ [46]. Принципиальная технологическая схема стадии утилизации отходов ПВХ второй очереди производства на Саянском ПО Химпром приведена на рис. 6.5. Корки из бункера-накопителя 1 непрерывно подаются на ленточный транспортер 2, снабженный устройством для сигнализации о металлических включениях. При попадании металлических предметов транспортер останавливается во избежание поломки ножей измельчителя. Корки Измельчаются в роторном измельчителе пластмасс 3 типа ИПР-300, а [c.171]
Если полученное значение и > (Ипр)2, то окончательно принимают и = (мпр)2- Если и [c.411]
Реакция превращения тиодигликоля в иприт может быть проведена при помощи обычных реагентов, которыми пользуются для получения галоидопроизводных из спиртов. В. Мейер — автор синтеза, для получения р-р -дихлордиэтилсульфида действовал на тиодигликоль треххлористым фосфором [c.147]
Впервые был получен немецким химиком В. Майером в 1886 г. Название вещество получило в честь бельгийского города Ипр, близ которого 13 июля 1917 г. оно впервые бьшо применено в качестве боевого ОВ. [c.812]
Монохлористая сера присоединяется к иприту, одновременно отщепляется свободная сера, которая всегда содержится в виде примеси в техническом иприте, полученном по этому способу. [c.95]
Этилен служит сырьем для получения винного спирта (см. с. 168) из него синтезируют крайне ядовитое отравляющее вещество — иприт. Интересно применение этилена в качестве вещества, ускоряющего созревание фруктов. [c.92]
Этилен служит сырьем для получения винного спирта (см. стр. 102) из него синтезируют крайне ядовитое отравляющее вещество — иприт (см. стр. 284). [c.78]
Иприт, или , j-дихлордиэтилсульфид, был впервые получен ученым Н. Д. Зелинским еще в 1887 г., когда он работал в Германии практикантом в лаборатории В. Майера. Работа с этим, неизвестным еще тогда соединением, едва не кончилась роковым образом для молодого Н. Д. Зелинского. Строение этого крайне токсичного соединения оказалось следующим [c.155]
Свободный хлор является отравляющим веществом (ОВ) удушающего действия. Его используют также для получения ОБ других категорий слезоточивых (хлорпикрин и др.) нарывных (иприт, люизит) удушающих (фосген).. [c.85]
Азотистый иприт Впервые получен в 1935 г. Около 30 ч [c.277]
Для проведения физических исследований были разработаны специальные виды образцов и электродов, которые обеспечивают однородность электрического поля и устранение краевых разрядов [4, с. 70 104]. Обычно считают, что значения S пp = = Ипр/Ь, полученные в условиях однородного поля при исключении частичных разрядов, характеризуют истинную ( внутреннюю ) электрическую прочность, поскольку они не зависят от [c.128]
Расход газа-посителя (гелий) — 40 см /мин чувствительность регистратора во время элюирования зоны пропана (масштаб 1 10) 1 = 0,25 см/мВ скорость движения диаграммной ленты Бг = 600 мм/ч = = 1 см/мин объем пробы ипр = 1 см (при 300,2 К) уровень флуктуационных помех /гмин/Б] = 0,01 мВ верхняя граница линейного диапазона, полученная при проведении серии анализов с увеличивающимся объемом пробы, /гмакс/61 = 400 мВ (это значение отвечает отклонению от линейной связи с размером пробы, равному 5%). [c.191]
Известны свидетельства того, что боевое применение отравляющих газов в период первой мировой войны имело значительную научную проработку как с точки зрения применения, так и в отношении последствий. В частности, в работах [Haber,1986 Goran,1967] описана роль известного немецкого ученого Фрица Хабера при подготовке и осуществлении газовой атаки при Ипре в 1915 г. (в качестве боевого вещества применялся хлор). Значение информации, полученной при анализе применения газов в качестве боевого отравляющего вещества, обсуждается при описании таких конкретных случаев и в гл. 18. [c.363]
Одним из наиболее важных сведений, полученных в ходе сравнения перемешивающих устройств, является влияние типа импеллера на качество алкилата. Как упоминалось выше, поскольку состав кислоты очень сильно влияет на качество алкилата, сравнение следует проводить при одинаковом составе кислоты. В настоящем исследовании ключевую роль в этом эффекте ипрали растворенные в кислоте углеводороды. Этот компонент, характеризующий силу кислоты, является сложной смесью с преобладанием в ней циклических полимеров [6]. Поскольку качество алкилата существенно меняется в зависимости от содержания в кислоте растворенных в ней углеводородов, было предложено много теорий, посвященных их роли в улучшении качества алкилата в некоторых из этих теорий им отводилась роль переносчиков гидрид-ионов, в других — роль поверхностно-активного вещества, в третьих —роль вещества, повышающего растворимость изобутана в серной кислоте. [c.184]
Большое значение имеет обеспечение гидрогенизационных установок водородом. Расход водорода зависит от условий процесса и состава перерабатываемого сырья. Чем выше давление процесса и содержание серы в сырье, тем больше расход водорода. Последний также тем выше, чем большую роль в процессе ипрает крекирующая функция катализатора. Меньше всего водорода рас-кодуется в процессах, где преобладает его гидрирующая функция. При переработке фракций из одной и той же нефти расход водорода возрастает по мере увеличения молекулярной массы этой фракции. Таким образом, основным назначением гидрогеншаци-онных процессов является переработка сернистых и высокосерни-стых нефтей с получением нефтепродуктов с малым количеством серосодержащих и других агрессивных соединений. В сочетании с другими вторичными процессами гидрогенизационные проц
www.chem21.info
Иприт — это… Что такое Иприт?
| Иприт | |
| Общие | |
|---|---|
| Систематическое наименование | Иприт, горчичный газ, b-дихлордиэтилсульфид, 2,2′-дихлордиэтиловый тиоэфир, 2,2′-дихлордиэтилсульфид, 1-хлор-2-(2′-хлорэтилтио)-этан |
| Сокращения | B |
| Химическая формула | C4H8Cl2S |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Молярная масса | 159 г/моль |
| Плотность | 1,280 г/см3 (15 °С) г/см³ |
| Термические свойства | |
| Температура плавления | 14,5 °C |
| Температура кипения | 217 °C |
| Химические свойства | |
| Растворимость в воде | 0,05 % г/100 мл |
Ипри́т (или горчичный газ, синонимы: 2,2′-дихлордиэтиловый тиоэфир, 2,2′-дихлордиэтилсульфид, 1-хлор-2-(2′-хлорэтилтио)-этан, «Лост») — химическое соединение с формулой S(CH2CH2Cl)2. Является боевым отравляющим веществом (ОВ) кожно-нарывного действия. (По другой классификации — ОВ цитотоксического действия, общего алкилирующего свойства.)
Получение
Иприт получают двумя способами:
- Из этилена CH2=CH2 и хлоридов серы, например S2Cl2 или SCl2:
- SCl2 + 2 C2H4 → (ClCH2CH2)2S
- Из тиодигликоля S(CH2CH2OH)2 и трихлорида фосфора PCl3:
- 3(HO-CH2CH2)2S + 2PCl3 → 3(Cl-CH2CH2)2S + 2P(OH)3
- или тиодигликоля и соляной кислоты:
- (HO-CH2CH2)2S + 2HCl → (Cl-CH2CH2)2S + 2H2O
Физические свойства
Иприт — бесцветная жидкость с запахом чеснока или горчицы. Технический иприт — тёмно-коричневая, почти чёрная жидкость с неприятным запахом. Температура плавления составляет 14,5 °C, температура кипения — 217 °C (с частичным разложением), плотность 1,280 г/см³ (при 15 °C).
Иприт легко растворяется в органических растворителях — галогеноалканах, бензоле, хлорбензоле — столь же хорошо, как и в растительных или животных жирах; растворимость в воде составляет 0,05 %. В то время, как растворимость в абсолютном этаноле выше 16 °С составляет почти 100 %, в 92 %-ном этаноле она едва достигает 25 %.
Вследствие некоторой поверхностной активности он уменьшает поверхностное натяжение воды и в небольшой мере растекается по ней тонким слоем, как плёнка масла. В результате добавления 1 % высокомолекулярного амина C22H38O2NH2 растекание иприта по воде увеличивается на 39 %.
Иприт очень медленно гидролизуется водой, скорость гидролиза резко возрастает в присутствии едких щелочей, при нагревании и перемешивании.
Иприт энергично реагирует с хлорирующими и окисляющими агентами. Так как при этом образуются нетоксичные продукты, указанные выше реакции используют для его дегазации. С солями тяжёлых металлов иприт образует комплексные окрашенные соединения; на этом свойстве основано обнаружение иприта.
Химические свойства
Иприт — это органическое соединение, которое имеет следующую формулу: (ClCH2CH2)2S.
При обычной температуре иприт представляет собой устойчивое соединение. При нагревании выше 170 °C он разлагается с образованием неприятно пахнущих ядовитых продуктов различного состава. При температуре выше 500 °C происходит полное термическое разложение. Кратковременное нагревание даже выше 300 °C почти не приводит к образованию продуктов разложения, поэтому иприт считается относительно устойчивым к детонации.
По отношению к металлам при обычной температуре иприт инертен, он почти не воздействует на свинец, латунь, цинк, сталь, алюминий; при повышении температуры сталь разрушается. Загрязнённый иприт, содержащий обычно воду и хлористый водород, вызывает коррозию стали. Образующиеся соли железа способствуют коррозии. Из-за выделяющихся газов (водорода, сероводорода, этилена и других продуктов разложения) следует считаться с повышением давления в закрытых ёмкостях, минах, бомбах и контейнерах для перевозки.
Ингибиторы коррозии и антиоксиданты препятствуют разложению при хранении. Такими веществами могут быть, например, галогениды тетраалкиламмония, гексаметилентетрамин, пиридин, пиколин, хинолин и другие органические аминопроизводные.
В организме человека иприт вступает в реакцию с NH группами нуклеотидов, которые входят в состав ДНК. Это способствует образованию сшивок между цепями ДНК, из-за чего данный участок ДНК становится неработоспособным.
Поражающее действие
Иприт воздействует на организм человека несколькими способами:
Канадский солдат после отравления ипритом.- разрушение клеточных мембран;
- нарушение обмена углеводов;
- «вырывание» азотистых оснований из ДНК и РНК.
Иприт обладает поражающим действием при любых путях проникновения в организм. Поражения слизистых оболочек глаз, носоглотки и верхних дыхательных путей проявляются даже при незначительных концентрациях иприта. При более высоких концентрациях наряду с местными поражениями происходит общее отравление организма. Иприт имеет скрытый период действия (2—8 ч) и обладает кумулятивностью.
В момент контакта с ипритом раздражение кожи и болевые эффекты отсутствуют. Поражённые ипритом места предрасположены к инфекции. Поражение кожи начинается с покраснения, которое проявляется через 2—6 ч после воздействия иприта. Через сутки на месте покраснения образуются мелкие пузыри, наполненные жёлтой прозрачной жидкостью, в последующем сливающиеся. Через 2—3 дня пузыри лопаются и образуется заживающая только через 20—30 суток язва. Если в язву попадает инфекция, то заживление может затянуться до 2—3 месяцев.
При вдыхании паров или аэрозоля иприта первые признаки поражения проявляются через несколько часов в виде сухости и жжения в носоглотке, затем наступает сильный отёк слизистой оболочки носоглотки, сопровождающийся гнойными выделениями. В тяжёлых случаях развивается воспаление лёгких, смерть наступает на 3—4-й день от удушья.
Особенно чувствительны к парам иприта глаза. При воздействии паров иприта на глаза появляется ощущение песка в глазах, слезотечение, светобоязнь, затем происходят покраснение и отёк слизистой оболочки глаз и век, сопровождающийся обильным выделением гноя.
Попадание в глаза капельно-жидкого иприта может привести к слепоте. При попадании иприта в желудочно-кишечный тракт через 30—60 мин. появляются резкие боли в желудке, слюнотечение, тошнота, рвота, в дальнейшем развивается понос (иногда с кровью).
Интересно отметить высказывания В.Мейера (Meyer V.[1]), который получил иприт в чистом виде в 1886 году:
«Сначала я склонялся к тому, что явления, наблюдающиеся при действии хлорида, следует объяснить особой восприимчивостью экспериментатора; однако в результате опытов, выполненных по моей просьбе в здешнем физиологическом институте, я уяснил нечто более важное. Согласно этим опытам, это соединение обладает в высокой степени опасными свойствами, как можно было заключить на основании предварительного, ограничивающегося наиболее важными и бросающимися в глаза наблюдениями, сообщения.
Каждого из кроликов средней величины дважды помещали на 3-4 часа в запертую клетку, вентилируемую сильным потоком воздуха. Перед попаданием в клетку поток воздуха проходил через стеклянную трубку, в которой находились полоски фильтровальной бумаги, смоченные 2,2′-дихлордиэтилсульфидом. Животные были возбуждены, часто касались лапами носа и морды, которые имели характерную ярко-красную окраску. Конъюнктива тоже покраснела, а глаза были очень влажными. Выделение влаги кожей заметно увеличилось. На следующий день глаза сильно воспалились, веки склеились гнойными выделениями. Появился сильный насморк, уши сильно опухли и в слуховом проходе появилось гнойное воспаление. К вечеру третьего дня животные умерли от острой пневмонии, распространившейся на оба легких. Один очень сильный кролик, который несколько часов вдыхал пары вещества через отверстие воздуховодной трубки, так что не действовали на поверхность тела, умер уже вечером того же дня от развившейся пневмонии, поэтому времени для проявления других симптомов уже не было. У кроликов, которым с помощью тонкой кисточки на неповрежденную кожу кончиков ушей было нанесено немного дихлодиэтилсульфида, на месте нанесения совершенно не появилось следов поражения, однако всё ухо сильно опухло, а в одном случае от основания слухового прохода до наружной части уха возникло обильное гнойное воспаление. Возможность затекания препарата в слуховой проход была исключена отчасти из-за незначительности нанесенного кисточкой количества вещества, отчасти вследствие того, что препарат был нанесён на наружную поверхность уха. В случае, когда кожу предварительно обнажали сбриванием шерсти с кончиков ушей, нанесённый кисточкой препарат, разумеется, вызывал преимущественное нагноение в этом месте, но одновременно и более сильное опухание всего уха и воспаление глаз. При подкожном введении примерно двух капель препарата в царапину на коже спины кролика возникало воспаление обоих глаз, очень сильный насморк и на третий день наступала смерть вследствие пневмонии. На месте нанесения препарата никаких признаков поражения не было. Так как пары вещества оказывали на экспериментатора вредное действие, подобное вкратце описанному выше, эти опыты пришлось прекратить.»
Минимальная доза, вызывающая образование нарывов на коже, составляет 0,1 мг/см². Лёгкие поражения глаз наступают при концентрации 0,001 мг/л и экспозиции 30 мин. Смертельная доза при действии через кожу 70 мг/кг (скрытый период действия до 12 ч и более). Смертельная концентрация при действии через органы дыхания в течение 1,5 ч — около 0,015 мг/л (скрытый период 4 — 24 ч).
Первая помощь при поражении ипритом
Антидота при отравлении ипритом пока не существует. Капли иприта на коже необходимо немедленно продегазировать с помощью индивидуального противохимического пакета. Глаза и нос следует обильно промыть, а рот и горло прополоскать 2 % раствором питьевой соды или чистой водой. При отравлении водой или пищей, заражённой ипритом, вызвать рвоту, а затем ввести кашицу, приготовленную из расчёта 25 г активированного угля на 100 мл воды. Язвы, образовавшиеся из-за попадания капель иприта на кожу, следует прижигать перманганатом калия (KMnO4).
Защитные средства
Для защиты органов дыхания и кожных покровов от действия иприта используются соответственно противогаз и специальная защитная одежда. Поскольку иприт обладает способностью диффундировать в сложные органические соединения, следует помнить, что ОЗК и противогаз не гарантируют полную защиту кожных покровов. Время нахождения в зоне поражения ипритом не должно превышать 40 минут, во избежание проникновения ОВ через средства защиты к коже.
История
Был синтезирован в Германии — Депре (в 1822 году) и (независимо) британским учёным Фредериком Гутри (Frederick Guthrie) в 1860 году[2]. Впервые иприт был применён Германией 12 июля 1917 года против англо-французских войск, которые были обстреляны минами, содержавшими маслянистую жидкость, у бельгийского города Ипр (откуда и произошло название этого вещества).
Во время Второй мировой войны иприт применялся только один раз Польшей, при этом погибли два немецких солдата, а двенадцать получили поражения разной степени тяжести[источник не указан 1309 дней]. Кроме того, иприт применялся во время подавления Синьцзянского восстания в 1934 году, в итало-эфиопскую войну 1935—1936 годов. В г. Дзержинске во время Второй мировой войны был секретный завод, на котором начиняли ипритом авиабомбы. Работники этого завода, получившие легочные поражения парами иприта, в послевоенное время вплоть до 90-х гг ХХ в. ежегодно проходили лечение в спецсанатории «Карасан» в 15 километрах к юго-западу от Алушты (между Алуштой и Ялтой)[источник не указан 584 дня].
Примечания
- ↑ Meyer V., Chem. Ber., Bd. 19, s. 326 (1886)
- ↑ Frederick Guthrie XIII.—On some derivatives from the olefines (англ.) // Quarterly Journal of the Chemical Society of London. — 1860. — Vol. 12. — № 1. — P. 109—126. — DOI:10.1039/QJ8601200109
Литература
- Франке З. Химия отравляющих веществ. М., «Химия», 1973, т. 1, стр.136.
- Соборовский Л. З., Эпштейн Г. Ю., Химия и технология боевых отравляющих веществ, М., 1938.
- Сартори М., Новое в химии боевых отравляющих веществ, «Успехи химии», 1954, т. 21, в. 1, с. 62.
- Эдуард Петрович Петренко. Военная токсикология, радиобиология и медицинская защита. — 2004. — 115 с.
Ссылки
test.academic.ru